Dị dạng động tĩnh mạch não (Brain arteriovenous malformations – AVMs) là sự thông nối (connections) mạch máu bất thường bên trong não, tình trạng mà có bản chất được cho là do bẩm sinh (congenital). Có một vài phân nhóm (subgroups), trong đó phổ biến nhất là AVM não dạng cuộn mạch (glomerular type), còn AVM não dạng rò (fistulous type) thì ít gặp hơn. AVM trong não (brain AVM) cũng có thể là một phần của bệnh lý lan rộng hơn (ví dụ: Hội chứng dị dạng động tĩnh mạch ở vùng mặt và não theo phân đoạn phôi thai – cerebrofacial arteriovenous metameric syndrome: CAMS).
Khi phát hiện các mạch máu bệnh lý nội sọ trên hình ảnh, cần phải xem xét đến các chẩn đoán khác, bao gồm: dị dạng phát triển tĩnh mạch (DVA – developmental venous anomalies) kích thước lớn, rò động tĩnh mạch màng cứng (dAVF – dural arteriovenous fistulas) nguy cơ cao (malignant) và bệnh moyamoya (moyamoya disease); vì các bệnh lý này có bản chất khác nhau và đòi hỏi các phương pháp điều trị khác nhau.
Một số dấu hiệu hình ảnh của dị dạng động tĩnh mạch não (AVM) có tác động đến việc đưa ra quyết định trong điều trị lâm sàng; quan trọng nhất là những dấu hiệu được biết là có liên quan đến nguy cơ xuất huyết (hemorrhage) trong tương lai, bao gồm: bằng chứng đã từng xuất huyết trước đó, phình mạch trong búi dị dạng nidus (intranidal aneurysms), hẹp tĩnh mạch (venous stenosis), dẫn lưu tĩnh mạch sâu (deep venous drainage) và vị trí búi dị dạng nidus nằm ở vùng sâu.
Các dấu hiệu hình ảnh khác cần được đưa vào bản báo cáo (report) chẩn đoán hình ảnh là những ảnh hưởng thứ phát gây ra bởi dị dạng động tĩnh mạch não (AVM), có thể dẫn đến các khiếm khuyết thần kinh không do xuất huyết, như: ứ trệ tĩnh mạch (venous congestion), tăng sinh tế bào thần kinh đệm (gliosis), não úng thủy (hydrocephalus), hoặc hiện tượng cướp máu động mạch (arterial steal).
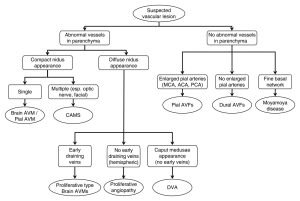
Hình 1: Sơ đồ minh họa cách tiếp cận chẩn đoán dựa trên hình ảnh học thực hành đối với các tổn thương nghi ngờ do mạch máu não. ACA = anterior cerebral artery: động mạch não trước, CAMS = cerebrofacial arteriovenous metameric syndrome: hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai, MCA = middle cerebral artery: động mạch não giữa, PCA = posterior cerebral artery: động mạch não sau.
Giới thiệu
Tổn thương mạch máu của não là tổn thương không thường gặp (uncommon lesions), có thể gây ra khó khăn trong chẩn đoán do chúng có những biểu hiện lâm sàng và đặc điểm hình ảnh tương tự nhau. Các hệ thống phân loại khác nhau đã được đưa ra. Hệ thống phân loại thường được sử dụng nhất chia các tổn thương mạch máu thành: dị dạng động tĩnh mạch (AVMs) – có thể thuộc màng mềm (pial) hoặc màng cứng (dural) tùy thuộc vào vị trí của luồng thông (shunt); u máu thể hang (cavernous hemangiomas = cavernomas); giãn mao mạch (capillary telangiectasia); và bất thường phát triển tĩnh mạch (DVAs – developmental venous anomalies) (trước đây gọi là u máu tĩnh mạch – venous angiomas).
Tuy nhiên, xét về mặt lâm sàng, hình ảnh học và tiên lượng, việc phân loại chi tiết hơn các bệnh lý khác nhau mà trước đây được xếp chung vào nhóm ‘dị dạng động tĩnh mạch não – brain AVMs’ dường như là cần thiết. Ngoài ra, với số lượng các trường hợp AVM não được phát hiện tình cờ ngày càng tăng, việc xác định chính xác tổn thương nào có xu hướng dễ dẫn đến xuất huyết hơn trong tương lai hoặc gây ra các triệu chứng thần kinh không do xuất huyết là rất quan trọng.
Các tổn thương có hình ảnh tương tự (mimics) với dị dạng động tĩnh mạch não (AVM) cần phải được nhận diện đúng bản chất để giúp định hướng chẩn đoán và điều trị. Thêm vào đó, khi phát hiện AVM não, các đặc điểm chi tiết cụ thể liên quan đến nguy cơ diễn tiến tự nhiên của AVM và các nguy cơ liên quan đến điều trị cần phải được nêu rõ trong bản báo cáo.
Nhiều tổn thương mạch máu có thể biểu hiện bằng các mạch máu bất thường trong não trên hình ảnh học và cần phải được chẩn đoán phân biệt với nhau, do chúng có diễn tiến tự nhiên (natural histories) và chiến lược điều trị khác nhau. Ví dụ: AVM não kinh điển và rò động tĩnh mạch màng mềm (pial AVFs – pial arteriovenous fistulas) nên được quản lý dựa trên nguy cơ liên quan đến bệnh lý so với nguy cơ liên quan đến điều trị; bất thường phát triển tĩnh mạch (DVAs) là biến thể bình thường (normal variants) và không bao giờ cần điều trị; rò động tĩnh mạch màng cứng (dural AVFs) có trào ngược tĩnh mạch vỏ não (cortical venous reflux) thì luôn luôn cần phải điều trị.
Trong bài viết này, chúng tôi trình bày cách tiếp cận chẩn đoán thực tiễn dựa trên hình ảnh học đối với các tổn thương mạch máu não nghi ngờ (Hình 1); thảo luận về các đặc điểm phân biệt của các loại dị dạng động tĩnh mạch não (AVM) khác nhau cũng như cách phân biệt giữa các tổn thương giả AVM não với AVM não thực sự; đồng thời mô tả các đặc điểm của AVM não cần phải được báo cáo để tạo điều kiện thuận lợi cho việc đưa ra quyết định điều trị.
Các mạch máu bất thường trong nhu mô não (Abnormal Intraparenchymal Vessels)
Dị dạng động tĩnh mạch não kinh điển (Classic Brain AVMs)
AVM não, hay cụ thể hơn là AVM trong nhu mô não hoặc trong màng mềm (pial AVMs), là sự thông nối bất thường giữa các động mạch bình thường cung cấp máu cho nhu mô não (tức là các mạch máu màng mềm) với các tĩnh mạch bình thường dẫn lưu máu cho não; kết quả là tạo ra luồng thông động tĩnh mạch (arteriovenous shunting) với một mạng lưới mạch máu trung gian nằm bên trong nhu mô não và không có giường mao mạch thật sự. Sự chuyển tiếp (transition) giữa động mạch và tĩnh mạch có thể diễn ra thông qua một cấu trúc gọi là búi dị dạng (nidus) (tức là một búi (tangle) mạch máu bất thường nằm trong nhu mô não) hoặc có thể là thông nối trực tiếp (tức là dạng rò – fistulous) mà không có bất kỳ mạng lưới trung gian nào. Trong trường hợp thông nối trực tiếp (dạng rò), thuật ngữ rò động tĩnh mạch não (brain arteriovenous fistula) hoặc rò động tĩnh mạch màng mềm (pial AVF) sẽ được sử dụng. Mặc dù AVM não là những tổn thương bẩm sinh, nhưng bệnh nhân có xu hướng biểu hiện triệu chứng muộn hơn trong cuộc đời, phổ biến nhất là xuất huyết nội sọ hoặc co giật.
Các đặc điểm hình ảnh của AVM não dạng búi dị dạng nidus là phù hợp với định nghĩa của nó. Tiêu chuẩn chẩn đoán bao gồm:
(a) sự hiện diện của một búi dị dạng nidus nằm trong nhu mô não, được xác định trên các phương pháp chẩn đoán hình ảnh (như CT, MRI) hoặc chụp mạch máu thông thường (conventional angiography); và (b) dẫn lưu tĩnh mạch sớm, dấu hiệu này được thấy rõ nhất trên các phương thức hình ảnh động học, tiêu chuẩn tham chiếu là chụp mạch máu thông thường qua ống thông (catheter).
Việc diễn giải rõ ràng về tình trạng dẫn lưu tĩnh mạch sớm chỉ có thể được thực hiện nếu các tĩnh mạch được nhìn thấy trong thì động mạch (“arterial” phase). Dấu hiệu này cũng có thể được nhận diện trên phim chụp cộng hưởng từ mạch máu (MRA) hoặc cắt lớp vi tính mạch máu (CTA) tiêu chuẩn nếu lưu lượng luồng thông và các tĩnh mạch dẫn lưu đủ lớn. Các phương thức hình ảnh như MRA động học (dynamic MRA) và CTA động học (dynamic CTA) ngày càng được sử dụng nhiều để phát hiện tình trạng dẫn lưu tĩnh mạch sớm cho các tổn thương nhỏ hơn, từ đó giúp thiết lập chẩn đoán, vì các tiêu chuẩn nêu trên là rất quan trọng để phân biệt AVM não với các bệnh lý mạch máu não khác.
Nếu có một búi dị dạng nidus thì có thể gặp hai phân nhóm của mạng lưới mạch máu bất thường này. Loại điển hình (typical type) là búi nidus dạng cuộn mạch (glomerular) hay dạng khối (compact), bao gồm các mạch máu bất thường mà không có bất kỳ nhu mô não bình thường nào xen kẽ bên trong (Hình 2, 3). Loại thứ hai hiếm gặp hơn được gọi là búi nidus dạng lan tỏa (diffuse) hoặc dạng tăng sinh (proliferative), trong đó nhu mô não bình thường nằm xen kẽ trong búi mạch máu (Hình 4). Nếu thấy dấu hiệu nhu mô não bình thường xen kẽ trong búi mạch máu bất thường thì bệnh lý mạch máu tăng sinh (proliferative angiopathy) hoặc hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai (CAMS) phải được đưa vào chẩn đoán phân biệt và có thể phân biệt chúng với AVM não thực sự dựa trên việc không có dấu hiệu dẫn lưu tĩnh mạch sớm được thấy trong bệnh lý mạch máu tăng sinh, và dựa vào vị trí kinh điển cũng như kết hợp với AVM vùng mặt trong CAMS.
Các động mạch nuôi và tĩnh mạch dẫn lưu của AVM não sẽ phụ thuộc vào vị trí của búi nidus. Búi nidus nằm ở sâu và trong não thất sẽ huy động các nhánh xuyên (perforator) (như nhánh thể vân (lentriculostriate), nhánh xuyên đồi thị (thalamoperforator)) và đám rối mạch mạc (choroidal) (các động mạch mạch mạc trước, sau trong và sau ngoài) tương ứng; trong khi đó, sự dẫn lưu tĩnh mạch thường sẽ thông qua hệ thống tĩnh mạch sâu (Hình 3).
Ở các vị trí nông hơn hoặc thuộc vỏ não, nguồn cấp máu động mạch chính thông qua các động mạch màng mềm (pial arteries) (các nhánh của động mạch não trước (ACA), não giữa (MCA) và não sau (PCA)); trong khi đó, sự dẫn lưu tĩnh mạch chủ yếu thông qua các tĩnh mạch vỏ não (Hình 2). Việc không có các tĩnh mạch dẫn lưu vỏ não của AVM não nằm nông có thể là dấu hiệu của tình trạng huyết khối (thrombosis) của các đường ra nằm nông, dẫn đến việc chuyển hướng dòng chảy vào hệ thống tĩnh mạch sâu; điều này gợi ý tổn thương không ổn định hơn.
Sự huy động nguồn cấp máu xuyên màng cứng (transdural supply) đôi khi được ghi nhận trong các tổn thương có kích thước lớn. Cần phải xác định xem nguồn cấp máu này đang nuôi nhu mô não bình thường (hệ quả của hiện tượng cướp máu động mạch dẫn đến thiếu máu cục bộ mạn tính của não bình thường, được bù trừ bởi nguồn cấp máu xuyên màng cứng), hay liệu nó đang nuôi chính AVM não hay không, điều mà có xu hướng thấy trong AVM não dạng nông có tiềm năng tăng sinh mạch (angiogenetic, proliferative).
Hình 2. AVM não kinh điển dạng nông (superficial type) ở bệnh nhân nam 18 tuổi, nhập viện với tình trạng tụ máu thùy đỉnh trái. (a) Hình ảnh CT mặt phẳng axial có tiêm thuốc tương phản cho thấy một búi các cấu trúc dạng ống bắt thuốc tương phản mạnh nằm trong thùy đỉnh trái; hình ảnh này phù hợp với một búi dị dạng nidus. Tình trạng tăng đậm độ biểu hiện cho xuất huyết trong não thất (intraventricular hemorrhage) cũng được ghi nhận bên trong các não thất.
(b) Hình ảnh cường độ tối đa (MIP – Maximum intensity projection) (hướng nhìn từ đáy sọ) từ dữ liệu CT mạch máu cho thấy sự giãn lớn của động mạch não giữa (MCA – middle cerebral artery) bên trái (so với bên phải); đây là động mạch cấp máu cho búi dị dạng nidus.
(c) Hình ảnh chụp mạch động mạch cảnh trong bên trái (hướng nghiêng) cho thấy một búi dị dạng nidus dạng cuộn mạch (glomerular) nằm ở vị trí vỏ não, được cấp máu chủ yếu bởi các nhánh đỉnh sau và nhánh góc của động mạch não giữa (MCA) bên trái; đồng thời ghi nhận dấu hiệu dẫn lưu sớm vào một tĩnh mạch vỏ não thùy đỉnh trái, các dấu hiệu này giúp xác định chẩn đoán AVM não.
Hình 3. AVM não dạng nằm sâu kinh điển ở bệnh nhân nữ 19 tuổi, nhập viện vì đau đầu đột ngột (sudden headaches) sau đó mất ý thức (loss of consciousness). Thăm khám thực thể (physical examination) ghi nhận tình trạng liệt (palsy) dây thần kinh sọ số VI hai bên. (a, b) Hình ảnh CT mặt phẳng axial trước tiêm (a) và sau tiêm thuốc tương phản (b) cho thấy các cấu trúc mạch máu bắt thuốc mạnh tại đồi thị bên trái. Mặc dù không thấy bằng chứng xuất huyết trên phim CT, nhưng lâm sàng vẫn nghi ngờ rất cao có tình trạng vỡ AVM. (c) Hình chụp mạch (angiogram) động mạch đốt sống bên trái hướng nghiêng giúp xác nhận sự hiện diện của AVM não ở đồi thị, được cấp máu bởi các nhánh mạch máu xuyên đồi thị và các nhánh mạch mạc sau bên trái; dẫn lưu chủ yếu vào tĩnh mạch Galen và một phần nhỏ vào tĩnh mạch thân nền của Rosenthal bên trái (các mũi tên). Ghi nhận các túi tĩnh mạch nhỏ (các đầu mũi tên), sự hiện diện của chúng gợi ý nguy cơ xuất huyết cao.
Hình 4. AVM não dạng tăng sinh (Proliferative type) ở bệnh nhân nữ 27 tuổi, có tiền sử đau đầu và co giật 6 năm. (a) Hình ảnh CT mặt cắt axial có tiêm thuốc tương phản cho thấy tổn thương mạch máu bắt thuốc tương phản ở thùy trán trái cạnh đường giữa, với các vùng đồng đậm độ khu trú bên trong đại diện cho nhu mô não bình thường nằm xen kẽ trong búi nidus. (b, c) Hình chụp mạch động mạch cảnh trong phải (b) và động mạch đốt sống trái (c) hướng nghiêng cho thấy búi nidus được cấp máu bởi các nhánh của cả hai động mạch não trước (ACA) và các nhánh thể chai sau bên trái; đồng thời có nguồn cấp máu màng não (leptomeningeal) từ các nhánh của động mạch não sau (PCA) trái và dẫn lưu tĩnh mạch sớm vào các tĩnh mạch vỏ não trán cạnh đường giữa, các dấu hiệu giúp xác định chẩn đoán AVM não. Ghi nhận các vùng thấu quang (radiolucent) bên trong búi nidus, phù hợp với tổn thương dạng tăng sinh (proliferative).
Hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai (Cerebrofacial Arteriovenous Metameric Syndrome – CAMS)
Hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai (CAMS) (còn được gọi là hội chứng Wyburn-Mason hoặc bệnh Bonnet-Dechaume-Blanc) là một trong những hội chứng mạch máu thần kinh theo phân đoạn (segmental), là kết quả của đột biến tế bào sinh dưỡng (somatic mutation) xảy ra trong vùng mào thần kinh (neural crest) hoặc trung mô đầu (cephalic mesoderm) lân cận, trước khi các tế bào tiền thân này di chuyển đến vị trí cuối cùng của chúng. Vì các tế bào con (daughter cells) mang đột biến được ‘phân bổ-seeded’ dọc theo các đường di chuyển đã xác định trước, nên sẽ gặp AVM có sự phân bố theo phân đoạn (segmental distribution) (có thể xuất hiện đồng thời (synchronously), hoặc thường gặp hơn là không đồng thời (metachronously)).
CAMS type 1 liên quan đến phần não trước trong (medial prosencephalon) và sẽ biểu hiện với AVM nằm ở thể chai (corpus callosum), vùng hạ đồi (hypothalamus) (tuyến yên – hypophysis) và mũi. CAMS type 2 liên quan đến phần não trước ngoài (lateral prosencephalon) với AVM tại thùy chẩm và đường dẫn truyền thị giác, bao gồm cả đồi thị (thalamus), võng mạc (retina) và hàm trên (maxilla) (Hình 5). CAMS type 3 liên quan đến não sau (rhombencephalon), và bệnh nhân bị ảnh hưởng sẽ có AVM tại tiểu não (cerebellum), cầu não (pons) và hàm dưới (mandible). Sự chồng lấp giữa các vùng phân bố này là phổ biến và sẽ tạo ra các kiểu hình hỗn hợp (mixed phenotypes).
Manh mối quan trọng nhất để chẩn đoán CAMS là sự hiện diện của nhiều AVM ở cả nhu mô não và vùng mặt. Các AVM não có sự phân bố đặc trưng như đã mô tả trước đó, và búi nidus dạng lan tỏa hoặc tăng sinh được cấp máu từ nhiều mạch máu xuyên nhỏ bàng hệ với luồng thông động tĩnh mạch khá chậm vào tĩnh mạch khiến cho việc điều trị các AVM này trở nên rất khó khăn. Nếu ghi nhận AVM não có các đặc điểm này trên phim chụp mạch não thường quy, cần thực hiện tiêm thuốc tương phản vào các động mạch cảnh ngoài để giúp đánh giá các dị dạng mạch máu tiềm ẩn tại vùng mắt, hàm trên-mặt hoặc hàm dưới.
Diễn tiến tự nhiên của AVM não liên quan đến CAMS dường như khác biệt so với AVM não kinh điển ở chỗ nó hiếm khi biểu hiện với xuất huyết. Tuy nhiên, các triệu chứng thần kinh có thể xuất hiện thông qua các cơ chế bệnh sinh khác, như não úng thủy tắc nghẽn (obstructive hydrocephalus) do các tĩnh mạch dẫn lưu hoặc do búi nidus của AVM não; co giật do tình trạng ứ trệ tĩnh mạch hệ quả từ quá trình huyết khối tiến triển của hệ thống tĩnh mạch dẫn lưu; và các khiếm khuyết thần kinh tiến triển do sự tăng kích thước của AVM theo thời gian.
Thông thường hơn, bệnh nhân sẽ nhập viện với các triệu chứng liên quan đến AVM vùng mặt, bao gồm mất thị lực tiến triển (progressive vision loss) dẫn đến mù lòa (blindness); chảy máu răng và nướu; và các vấn đề về thẩm mỹ (cosmetic) (ví dụ: mặt không đối xứng). Tình trạng chảy máu tái phát từ AVM vùng hàm trên và hàm dưới thường rất nghiêm trọng, và can thiệp nội mạch là lựa chọn tốt nhất trong bệnh cảnh cấp cứu (Hình 6). Tuy nhiên, phẫu thuật cắt bỏ (bất cứ khi nào có thể) vẫn là phương pháp điều trị được lựa chọn đối với AVM vùng mặt.
Hình 5. Hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai (CAMS) type 2 ở bé gái 10 tuổi, nhập viện với tiền sử yếu nửa người phải (right hemiparesis) tiến triển trong vòng 1 năm. Ghi nhận thêm tình trạng phù kết mạc (chemosis) và lồi mắt (proptosis) bên trái. (a, b) Hình ảnh CT có tiêm thuốc tương phản mặt phẳng axial ngang mức hốc mắt (a) và não (b) cho thấy tổn thương mạch máu bắt thuốc tại hạch nền trái. Tổn thương gây hiệu ứng khối (mass effect) chèn ép não thất bên bên trái. Ngoài ra, ghi nhận các cấu trúc ngoằn ngoèo (serpiginous) bao quanh dây thần kinh thị giác. (c) Hình ảnh chụp mạch động mạch cảnh trong trái hướng nghiêng cho thấy búi nidus AVM não dạng tăng sinh (proliferative type) tại vùng hạch nền (basal ganglia). Một AVM nhỏ hơn khác được ghi nhận bao quanh dây thần kinh thị trái (mũi tên đặc). Có sự dẫn lưu tĩnh mạch sớm ra phía trước vào các tĩnh mạch vỏ não thùy trán nền (các đầu mũi tên) và ra phía sau vào tĩnh mạch nền của Rosenthal (mũi tên rỗng).
Hình 6. Hội chứng dị dạng động tĩnh mạch vùng mặt và não theo phân đoạn phôi thai (CAMS) type 2 ở bé gái 7 tuổi, nhập viện vì các đợt chảy máu nướu răng tái phát do mọc răng hàm bên trái. (a) Hình ảnh CT mặt phẳng coronal (cửa sổ xương) cho thấy một tổn thương hủy xương (osteolytic) bên trong gờ xương ổ răng của xương hàm trên bên trái. (b, c) Hình ảnh chụp mạch động mạch cảnh ngoài (b) và cảnh trong (c) bên trái cho thấy AVM xương mặt (facial osseous AVM) được cấp máu bởi các nhánh của động mạch hàm trong (internal maxillary) và động mạch mặt ngang (transverse facial) dẫn lưu vào một túi tĩnh mạch trong xương (mũi tên ở hình b). Dấu hiệu này tương ứng với tổn thương hủy xương (osteolytic) được thấy ở hình (a) và được chứng minh là nguyên nhân gây chảy máu của bệnh nhân. AVM của dây thần kinh thị giác bên trái cũng được ghi nhận, từ đó cho phép chẩn đoán xác định CAMS type 2. Trong trường hợp này, việc thuyên tắc mạch (embolization) cấp cứu AVM vùng mặt đã được thực hiện để cầm máu.
Bệnh lý mạch máu tăng sinh (Proliferative Angiopathy)
Bệnh lý mạch máu tăng sinh ở não (Cerebral proliferative angiopathy), trước đây được gọi là AVM loại nidus lan tỏa (diffuse nidus type AVM), chiếm khoảng 2%–4% tổng số các ca AVM não. Đây được xem là một bệnh lý riêng biệt so với AVM não kinh điển. Bệnh có xu hướng gặp ở nữ giới với tỷ lệ 2:1, và độ tuổi trung bình của bệnh nhân khá trẻ (20 tuổi).
Khiếm khuyết thần kinh tiến triển, cơn thiếu máu não cục bộ thoáng qua (TIA), co giật và đau đầu là các triệu chứng biểu hiện thường gặp, trong khi xuất huyết lại cực kỳ hiếm thấy. Mặc dù nguyên nhân của bệnh vẫn chưa được làm rõ, nhưng bệnh lý này đặc trưng bởi tình trạng tăng sinh nội mô và tăng sinh mạch. “Búi dị dạng nidus” bao gồm nhiều động mạch, được hình thành như một phản ứng tăng sinh mạch đối với tình trạng thiếu máu cục bộ vỏ não.
Các dấu hiệu điển hình trên MRI và CT bao gồm búi nidus dạng tăng sinh, trong đó nhu mô não bình thường nằm xen kẽ giữa các mạch máu bất thường. Thông thường, tổn thương sẽ ảnh hưởng đến toàn bộ một thùy não hoặc thậm chí là cả một bán cầu não (Hình 7). Khi chụp mạch máu não (cerebral angiography), các động mạch nuôi có xu hướng có kích thước bình thường hoặc chỉ giãn trung bình. Các vị trí hẹp của động mạch nuôi thường được ghi nhận kèm theo, và có nguồn cấp máu xuyên qua màng cứng lan rộng cho nhu mô não bình thường và bất thường từ các nhánh của động mạch cảnh ngoài (ECA). Không thấy hình ảnh dẫn lưu tĩnh mạch sớm rõ ràng trên các chuỗi hình ảnh động là yếu tố then chốt để phân biệt bệnh lý này với AVM não kinh điển.
Vì cơ chế bệnh sinh của bệnh lý mạch máu tăng sinh chủ yếu do thiếu máu cục bộ vỏ não (đã được chứng minh qua các phương thức hình ảnh về tưới máu não), nên đã có những báo cáo về việc điều trị thành công bằng phẫu thuật đắp động mạch lên màng mềm (pial synangiosis) hoặc tạo lỗ khoan sọ (burr-hole) để tăng cường nguồn cấp máu cho mô não lành từ động mạch cảnh ngoài.
Hình 7. Bệnh lý mạch máu tăng sinh (Proliferative angiopathy) ở bệnh nhân nam 26 tuổi với tiền sử yếu nửa người trái tiến triển đã 6 năm.
Hình (a, b): Hình ảnh MRI xung PD (proton-density–weighted) (a) và T1W sau tiêm thuốc tương phản Gadolinium (b) mặt phẳng axial cho thấy nhiều cấu trúc dạng ống với hình ảnh trống tín hiệu của dòng chảy (flow voids) và bắt thuốc tương phản, biểu hiện cho tổn thương mạch máu lớn lan tỏa toàn bộ bán cầu não phải. Nhu mô não bình thường nằm xen kẽ giữa các mạch máu bất thường này.
(c) Hình ảnh chụp mạch động mạch cảnh trong phải hướng trước-sau cho thấy các nhánh của động mạch não giữa (MCA) có kích thước tương đối bình thường và không có hiện tượng dẫn lưu tĩnh mạch sớm; những dấu hiệu này giúp xác định chẩn đoán bệnh lý mạch máu tăng sinh. Hẹp đoạn gần M2 của động mạch não giữa phải, ngay sau chỗ chia đôi của MCA (mũi tên).
(d) Hình ảnh chụp mạch động mạch cảnh ngoài phải hướng nghiêng cho thấy nguồn cấp máu xuyên màng cứng (transdural supply) lan rộng cho bán cầu não phải thông qua các nhánh của động mạch màng não giữa. Động mạch não sau (PCA) bên trái (không hiển thị hình) cũng bị ảnh hưởng.
Bất thường phát triển tĩnh mạch (Developmental Venous Anomalies)
Mặc dù không được phân loại là AVM, nhưng bất thường phát triển tĩnh mạch (DVA) có thể biểu hiện trên hình ảnh với đám rối mạch máu nằm trong nhu mô, đại diện cho những biến thể hình thái đặc biệt của hệ thống tĩnh mạch xuyên não bình thường. Mặc dù hầu hết các trường hợp DVA đều không có triệu chứng, chúng có thể có triệu chứng với tình trạng thiếu máu cục bộ (ischemia) hoặc nhồi máu (infarctions) tĩnh mạch nếu dòng chảy ra (outflow) của tĩnh mạch bàng hệ bị tổn thương.
DVA được cho là sự thích nghi đối với ‘các tai nạn – accidents’ xảy ra trong quá trình tạo phôi thai (embryogenesis) giữa giai đoạn phát triển phôi thứ tư và thứ bảy (tương ứng với khoảng chiều dài phôi từ 40–80 mm) như mô tả của nhà thần kinh phôi thai học D. H. Padget trong nghiên cứu năm 1948. Những sự cố này dẫn đến tình trạng tắc nghẽn (occlusion) hoặc kém phát triển (maldevelopment) của hệ thống tĩnh mạch nông (superficial) hoặc tĩnh mạch sâu (deep). Do khả năng biến đổi linh hoạt (plasticity) của hệ thống mạch máu ở giai đoạn này, DVA được hình thành như các con đường bù trừ, thông qua việc huy động và làm giãn các tĩnh mạch xuyên tủy (transmedullary veins) đã có sẵn từ trước.
Trên hình ảnh CT và MRI, tĩnh mạch dẫn lưu chính (venous collector) có thể được biểu hiện dưới dạng cấu trúc dạng đường thẳng hoặc đường cong có bắt thuốc hoặc trống tín hiệu của dòng chảy (flow void). Hình ảnh bắt thuốc của các tĩnh mạch tủy bị giãn (hình đầu rắn Medusa – ‘caput medusae’) cũng có thể được quan sát thấy. Có thể dễ dàng phân biệt DVA kích thước lớn với AVM não dựa trên kết quả chụp mạch não (cerebral angiography). Đặc điểm hình ảnh chụp mạch kinh điển là hình ảnh đầu sứa Medusa (hay còn gọi là ‘chiếc ô ngược – inverse umbrella’) của các tĩnh mạch xuyên tủy (vốn chỉ quan sát được ở thì tĩnh mạch) dẫn lưu vào tĩnh mạch dẫn lưu chính (venous collector), sau đó tĩnh mạch này sẽ tiếp tục dẫn lưu vào hệ thống tĩnh mạch nông hoặc tĩnh mạch sâu (Hình 8).
Ở những tổn thương kích thước lớn hơn có thể quan sát thấy vùng bắt thuốc mạnh của mao mạch dày đặc (dense capillary stain); tuy nhiên, việc không có sự giãn ra của động mạch sẽ gợi ý chẩn đoán là DVA. Trong những trường hợp ngoại lệ, các tĩnh mạch của ‘đầu sứa Medusa’ có thể xuất hiện sớm hơn một chút (tức là ở thì mao mạch muộn) do thời gian chuyển tiếp qua mao mạch nhanh hơn vì sự giãn ra của các khoang mao mạch, dấu hiệu này không nên hiểu sai (misinterpreted) là luồng thông động-tĩnh mạch (arteriovenous shunt).
Vì DVA hiếm khi gây chảy máu, nên nếu DVA được phát hiện trên hình ảnh dường như là nguyên nhân gây ra xuất huyết trong nhu mô, thì phải tìm kiếm u máu dạng hang (cavernoma) phối hợp đi kèm; tổn thương này có thể được quan sát tốt nhất trên các chuỗi xung Gradient-echo (GRE) hoặc các chuỗi xung phụ thuộc nồng độ oxy trong máu.
Hình 8. Bất thường phát triển tĩnh mạch (DVA) ở bệnh nhân nam 25 tuổi, nhập viện với triệu chứng đau đầu và tình cờ phát hiện tổn thương mạch máu. (a) Hình ảnh MRI chuỗi xung T1W sau tiêm thuốc tương phản Gadolinium mặt phẳng Sagittal cho thấy nhiều cấu trúc dạng ống bắt thuốc mạnh, tập trung chủ yếu ở thân não (brainstem) và thùy nhộng (vermis), xen kẽ với nhu mô não bình thường. Một số DVA có hình dạng đầu sứa Medusa (caput medusae), nhưng do kích thước lớn, tổn thương trong trường hợp này rất khó phân biệt với AVM não nếu chỉ dựa trên các dấu hiệu hình ảnh MRI đơn thuần.
(b, c) Hình ảnh chụp mạch động mạch đốt sống trái hướng nghiêng ở thì động mạch muộn (b) và thì tĩnh mạch (c) cho thấy vùng bắt thuốc mạnh của mao mạch dày đặc bên trong thân não và thùy nhộng; tuy nhiên, không ghi nhận tình trạng giãn động mạch hay dẫn lưu tĩnh mạch sớm. Hình ảnh đầu sứa Medusa của các tĩnh mạch xuyên tủy dẫn lưu vào nhiều tĩnh mạch dẫn lưu chính (venous collectors) được quan sát thấy rõ ràng trên hình ảnh ở thì tĩnh mạch.
Các mạch máu bất thường ngoài nhu mô não (Abnormal Extraparenchymal Vessels)
Rò động tĩnh mạch màng mềm (Pial Arteriovenous Fistulas – Pial AVFs)
Mặc dù thuộc nhóm AVM màng mềm “thực sự – true”, rò động tĩnh mạch màng mềm (pial AVFs) không biểu hiện hình ảnh búi mạch máu (tangle of vessels) trong nhu mô não kinh điển. Rò động tĩnh mạch màng mềm (pial AVFs) đại diện cho một phân nhóm đặc biệt của các luồng thông động tĩnh mạch não và chiếm khoảng 5% trong tổng số các trường hợp AVM não. Chúng tạo thành các shunt động tĩnh mạch màng mềm thực sự và bao gồm sự thông nối rò trực tiếp giữa một động mạch màng mềm và một tĩnh mạch mà không có bất kỳ búi dị dạng nidus nào ở giữa.
Rò động tĩnh mạch màng mềm (Pial AVFs) nằm trên bề mặt não, thường là các tổn thương có lưu lượng cao, và trong hầu hết các trường hợp đều đi kèm với các túi tĩnh mạch giãn (dilated venous pouches). Rò động tĩnh mạch màng mềm (Pial AVFs) thường gặp hơn ở trẻ em và thường xuyên liên quan đến giãn mao mạch xuất huyết di truyền (hereditary hemorrhagic telangiectasia – HHT).
Các manh mối (Clues) để chẩn đoán rò động tĩnh mạch màng mềm (Pial AVF) trên hình ảnh bao gồm sự hiện diện của: (a) các mạch máu giãn, chủ yếu nằm ở bề mặt não; và (b) sự giãn ra không đối xứng của động mạch nuôi màng mềm (pial feeding artery) — có thể là động mạch não giữa (MCA), động mạch não trước (ACA), hoặc động mạch não sau (PCA) — điều này được quan sát tốt nhất ở ngang mức đa giác Willis. Những dấu hiệu này có thể được sử dụng để phân biệt rò động tĩnh mạch màng mềm (Pial AVF) với rò động tĩnh mạch màng cứng (Dural AVF) (Hình 9) và có thể đi kèm với các túi tĩnh mạch giãn nằm ngoài nhu mô não.
Hình 9. Rò động tĩnh mạch màng mềm (Pial AVF) ở trẻ sơ sinh 1 tuần tuổi nhập viện với tình trạng suy tim sung huyết (congestive heart failure). Bệnh nhân có tiền sử gia đình mắc bệnh giãn mao mạch xuất huyết di truyền (hereditary hemorrhagic telangiectasia – HHT). (a, b) Hình ảnh MRI xung T2W mặt phẳng axial cho thấy giãn động mạch não giữa (MCA) bên phải ở ngang mức đa giác Willis (mũi tên ở hình a) và một cấu trúc mạch máu giãn lớn ở vùng quanh rãnh Sylvius phải (đầu mũi tên ở hình b), các dấu hiệu này gợi ý một túi tĩnh mạch (venous pouch). Phần trên của một cấu trúc trống tín hiệu dòng chảy (flow void) lớn khác cũng được quan sát thấy ở hố sau. Không tìm thấy búi dị dạng nidus.
(c) Hình ảnh chụp mạch động mạch cảnh trong phải hướng nghiêng cho thấy một lỗ rò lưu lượng cao (high-flow fistula) giữa một nhánh của động mạch não giữa (MCA) và một túi tĩnh mạch lớn (đầu mũi tên). Dòng chảy ngược (retrograde flow) của thuốc tương phản vào động mạch thân nền (basilar artery) xác nhận sự hiện diện của một lỗ rò lưu lượng cao khác (các mũi tên) từ động mạch tiểu não sau dưới (PICA). Các lỗ rò lưu lượng cao và túi tĩnh mạch là những dấu hiệu điển hình ở bệnh nhân bị giãn mao mạch xuất huyết di truyền (HHT).
Rò động tĩnh mạch màng cứng (Dural Arteriovenous Fistulas – DAVFs)
Rò động tĩnh mạch màng cứng (Dural AVFs) là các thông nối bất thường giữa các động mạch (vốn bình thường sẽ cấp máu cho màng não, xương hoặc cơ, chứ không phải cấp máu cho não) và các tiểu tĩnh mạch nhỏ (small venules) nằm bên trong màng cứng (dura mater). Chúng chiếm khoảng 10%–15% tổng số các luồng thông động tĩnh mạch nội sọ. Cách đơn giản nhất để phân loại các tổn thương này là nhóm chúng thành hai loại: có trào ngược tĩnh mạch vỏ não và không có trào ngược tĩnh mạch vỏ não. Nhóm không có trào ngược tĩnh mạch vỏ não là các lỗ rò lành tính (benign fistulas) (Borden type 1), hầu như không bao giờ dẫn đến các khiếm khuyết thần kinh, trong khi nhóm có trào ngược tĩnh mạch vỏ não được xem là các lỗ rò nguy cơ cao (malignant fistulas) (Borden type 2 và 3). Trường hợp rò động tĩnh mạch màng cứng nguy cơ cao (Malignant dural AVFs) thường có diễn tiến lâm sàng rầm rộ, bao gồm xuất huyết nội sọ, co giật, sa sút trí tuệ, rối loạn ý thức và các triệu chứng thần kinh khu trú không do xuất huyết do tình trạng ứ trệ tĩnh mạch hoặc vỡ các túi tĩnh mạch.
Rò động tĩnh mạch màng cứng (Dural AVF) có trào ngược tĩnh mạch vỏ não (cortical venous reflux) sẽ biểu hiện bằng các mạch máu bất thường nằm bên ngoài nhu mô não và cần phải được chẩn đoán phân biệt với các luồng thông mạch máu khác (sẽ được mô tả ở phần sau). Các dấu hiệu trên CT và MRI bao gồm giãn các tĩnh mạch vỏ não (một tình trạng được một số tác giả gọi là dạng giả tĩnh mạch bệnh lý – pseudophlebitic pattern), biểu hiện bằng các cấu trúc dạng ống bắt thuốc bất thường hoặc các vùng trống tín hiệu dòng chảy (flow voids) bên trong các rãnh vỏ não (cortical sulci), mà không có búi dị dạng nidus thực sự bên trong nhu mô não (Hình 10).
Tình trạng giảm đậm độ (Hypoattenuation) của chất trắng trên CT hoặc tăng tín hiệu (hyperintense) ở xung T2W trên MRI cho thấy tình trạng ứ trệ tĩnh mạch hoặc nhồi máu, những yếu tố này cuối cùng có thể dẫn đến xuất huyết tĩnh mạch. Sự bắt thuốc khu trú tại các vùng này cũng có thể được quan sát thấy như một dấu hiệu của tình trạng thiếu máu cục bộ tĩnh mạch mạn tính. Trên CT, có thể thấy vôi hóa dưới vỏ não dạng đường cong ở những bệnh nhân có trào ngược tĩnh mạch vỏ não kéo dài, khả năng cao là do hậu quả của tình trạng ứ trệ tĩnh mạch mạn tính.
Tuy nhiên, chỉ riêng hình ảnh cắt lớp (CT, MRI) thường không đủ để xác định chính xác vị trí của rò động tĩnh mạch màng cứng (Dural AVF). Các hình ảnh động học với chụp cộng hưởng từ động mạch (MRA – MR angiography), cắt lớp vi tính động mạch (CTA – CT angiography), hoặc chụp mạch số hóa xóa nền (digital subtraction angiography (DSA) – tiêu chuẩn để tham chiếu) sẽ giúp hiển thị tình trạng lấp đầy tĩnh mạch sớm, sự tham gia của các nhánh động mạch cảnh ngoài (không phải các mạch máu màng mềm), và vị trí của luồng thông (shunt). Điều trị là bắt buộc đối với các trường hợp rò động tĩnh mạch màng cứng nguy cơ cao (malignant dural AVFs) vì diễn tiến tự nhiên rất xấu nếu không được xử trí.
Hình 10. Rò động tĩnh mạch màng cứng (Dural AVF) type 2 theo phân loại Borden ở bệnh nhân nữ 45 tuổi nhập viện do mất ý thức (loss of consciousness) đột ngột. (a) Hình ảnh CT mặt phẳng axial không tiêm thuốc cho thấy khối máu tụ (hematoma) vùng thái dương – chẩm trái kèm theo xuất huyết trong não thất (intraventricular hemorrhage). (b) Hình ảnh MRI xung T2W mặt phẳng axial cho thấy nhiều cấu trúc mạch máu trống tín hiệu của dòng chảy (flow voids) dọc theo các rãnh vỏ não ở cả hai vùng chẩm. Có tình trạng phù chất trắng với tăng tín hiệu trên T2W ở thùy chẩm trái, cùng với bằng chứng của khối máu tụ đang trong giai đoạn thoái triển. Không tìm thấy búi dị dạng nidus.
(c) Hình ảnh chụp mạch động mạch hàm trên trong (internal maxillary angiogram) bên trái cho thấy rò động tĩnh mạch màng cứng (Dural AVF) tại xoang ngang (transverse sinus) bên trái, được cấp máu bởi các nhánh của động mạch màng não giữa trái. Ghi nhận huyết khối (thrombosis) kèm theo ở các đoạn gần và đoạn xa của xoang ngang, tạo thành một “túi tách biệt – isolated pouch” và từ đó gây ra tình trạng trào ngược từ luồng thông (shunt) vào các tĩnh mạch vỏ não.
Bệnh moyamoya (Moyamoya Disease)
Bệnh moyamoya (“moyamoya” trong tiếng Nhật có nghĩa là ‘đám khói – puff of smoke’) là bệnh lý tắc nghẽn động mạch hiếm gặp không rõ nguyên nhân. Theo kinh điển, bệnh liên quan đến động mạch cảnh trong đoạn trên mỏm yên (supraclinoid) và thường không ảnh hưởng đến vùng hố sau trong các giai đoạn sớm.
Thuật ngữ hội chứng moyamoya (moyamoya syndrome) được sử dụng trong những trường hợp có nguyên nhân nền (như xơ vữa động mạch (atherosclerosis), hội chứng Down (Down syndrome), bệnh lý u sợi thần kinh (neurofibromatosis), bệnh hồng cầu hình liềm (sickle cell disease) hoặc các bệnh lý khác). Thường có sự phát triển lan rộng của các động mạch xuyên bàng hệ rất nhỏ ở nền sọ (mạch máu moyamoya), vốn được mô tả là có hình ảnh ‘đám khói – puff of smoke’ trên phim chụp mạch não (cerebral angiography), và các động mạch bàng hệ xuyên màng cứng. Biểu hiện lâm sàng khác nhau giữa trẻ em và người lớn: Hầu hết trẻ em nhập viện vì cơn thiếu máu cục bộ não thoáng qua (TIA – transient ischemic attack) hoặc nhồi máu não (cerebral infarctions); trong khi đó, khoảng một nửa số người lớn biểu hiện tình trạng xuất huyết nội sọ do vỡ các mạch máu bàng hệ moyamoya.
Các manh mối hình ảnh trên CT và MRI bao gồm sự hiện diện của các vùng trống tín hiệu của dòng chảy (flow voids) rất nhỏ (tiny), thường thấy xuất phát từ các bể nền (basal cisterns) và lan vào hạch nền (basal ganglia) hoặc đồi thị (thalamus). Không có búi dị dạng nidus thực sự nằm trong nhu mô não và không có các mạch máu giãn (Hình 11). Mặc dù chẩn đoán có thể được gợi ý bởi sự hiện diện của tình trạng hẹp động mạch cảnh trong đoạn trên yên hai bên trên hình chụp MRA và CTA, nhưng chụp mạch não (cerebral angiography) vẫn cần thiết để đánh giá tiền phẫu cho việc tái thông mạch máu (revascularization) trong bệnh Moyamoya. Rất nhiều các con đường bàng hệ thứ phát (bao gồm các động mạch xuyên bàng hệ moyamoya ở nền sọ, nguồn cấp máu xuyên màng cứng từ các động mạch màng não giữa đến vùng lồi của não (convexity), và thông qua động mạch mắt (ophthalmic artery) đến các nhánh của động mạch não trước) thường chỉ có thể được đánh giá bằng chụp mạch số hóa xóa nền (DSA) do kích thước nhỏ của chúng.
Các nghiên cứu gần đây đã chỉ ra rằng cộng hưởng từ tưới máu (perfusion MRI) và các phương thức hình ảnh về dự trữ mạch máu não (CVR – cerebrovascular reserve) có thể hữu ích cho việc phân loại bệnh nhân trước phẫu thuật và theo dõi hậu phẫu sau phẫu thuật tái thông mạch máu.
Hình 11. Bệnh Moyamoya ở bệnh nhân nữ 28 tuổi từng bị hai đợt xuất huyết nội sọ tái phát. (a) Hình ảnh CT mặt phẳng axial cho thấy tình trạng xuất huyết trong não thất. (b) Hình ảnh MRI xung T2W mặt phẳng axial cho thấy các vùng trống tín hiệu của dòng chảy (flow voids) rất nhỏ bên trong bể quanh trung não (perimesencephalic cistern) và bao quanh não giữa (midbrain). Không ghi nhận hình ảnh búi dị dạng nidus. (c) Hình ảnh chụp mạch động mạch cảnh chung trái hướng trước – sau cho thấy tình trạng tắc nghẽn động mạch cảnh trong đoạn trên mỏm yên (mũi tên đặc) cùng với các động mạch xuyên bàng hệ rất nhỏ (các đầu mũi tên). Ngoài ra còn ghi nhận nguồn cấp máu bàng hệ xuyên màng cứng từ động mạch màng não giữa (mũi tên rỗng). (d) Hình ảnh chụp mạch động mạch đốt sống trái hướng trước – sau cho thấy sự ảnh hưởng cả hai bên của các động mạch não sau (PCA); điều này cùng với việc thiếu tương đối các mạch máu bàng hệ dạng đám khói (puff-of-smoke collateral vessels) gợi ý bệnh đang ở giai đoạn muộn.
Đánh giá và quản lý điều trị dị dạng động tĩnh mạch não (Assessment and Management of Brain AVMs)
Hình ảnh dị dạng động tĩnh mạch não (Imaging of Brain AVMs):
Những điều mà bác sĩ lâm sàng cần biết:
Sau khi đã xác định chẩn đoán là dị dạng động tĩnh mạch (AVM) não thực sự, cần phải trả lời một số câu hỏi liên quan đến nguy cơ dự đoán (anticipated risk) các khiếm khuyết thần kinh (bao gồm cả do xuất huyết và không do xuất huyết) cũng như các nguy cơ dự đoán liên quan đến quá trình điều trị.
Trong số các biến chứng liên quan đến AVM não, xuất huyết nội sọ là điều đáng lo ngại nhất. Do đó, nhiều nghiên cứu khác nhau đã tìm cách xác định những yếu tố nào có liên quan đến nguy cơ xuất huyết cao hơn trong tương lai. Các đặc điểm được tóm tắt trong Bảng 1 đã được xác định là có liên quan đến nguy cơ cao hơn gây ra các khiếm khuyết thần kinh do xuất huyết và không do xuất huyết, và đó là điều quan trọng mà bác sĩ lâm sàng cần biết.
Đối với bệnh nhân có AVM não nhập viện vì chảy máu cấp tính (acute bleeding), dấu hiệu quan trọng nhất cần phải thông báo khẩn cấp cho bác sĩ lâm sàng (ngoài các dấu hiệu đe dọa tính mạng (life-threatening) như đẩy lệch đường giữa hoặc thoát vị não) là sự hiện diện của phình mạch trong búi nidus (intranidal aneurysms) hoặc túi phình tĩnh mạch (venous pouches) (Hình 3, 12), do nguy cơ xuất huyết tái phát sớm cao hơn.
Vì tiền sử xuất huyết trước đó là yếu tố dự đoán quan trọng và nhất quán nhất cho các đợt xuất huyết trong tương lai, nên trong bối cảnh phát hiện tình cờ AVM não, bước đầu tiên cần làm là phân biệt giữa nhóm AVM não đã từng chảy máu và nhóm AVM não chưa từng chảy máu; điều mà trong hầu hết các trường hợp có thể thực hiện được thông qua việc xem xét bệnh sử lâm sàng. Các chuỗi xung Gradient-echo T2W (T2*), có độ nhạy cao trong việc phát hiện các dấu hiệu của xuất huyết cũ, có thể giúp xác định những bệnh nhân cực kỳ hiếm gặp là không triệu chứng đã từng có xuất huyết dưới lâm sàng (subclinical hemorrhage).
Ngoài ra, các điểm yếu (weak points) về cấu trúc mạch máu cụ thể phải được đưa vào trong bản báo cáo hình ảnh, vì chúng có thể làm tăng nguy cơ xuất huyết trong tương lai. Phình mạch trong búi nidus (Intranidal aneurysms), giãn tĩnh mạch (venous ectasias), hẹp tĩnh mạch (venous stenosis), dẫn lưu tĩnh mạch sâu, dẫn lưu tĩnh mạch đơn độc và các vị trí ở hố sau đều tạo thành các điểm yếu về cấu trúc mạch máu. Lớn tuổi và nam giới cũng có thể làm tăng nguy cơ xuất huyết. Mặc dù nguyên tắc này chưa được chứng minh qua các thử nghiệm tiền cứu ngẫu nhiên, nhưng chúng tôi đã sử dụng nó trong thực hành lâm sàng suốt hơn 20 năm và đã ghi nhận kết cục cải thiện rõ rệt trong quá trình theo dõi so với diễn tiến tự nhiên của bệnh.
Tuy nhiên, việc điều trị có thể được chỉ định đối với AVM chưa vỡ và không biểu hiện các điểm yếu của cấu trúc mạch máu. Trong số đó, shunt lưu lượng cao có thể dẫn đến chậm phát triển tâm thần vận động (psychomotor developmental retardation) và suy tim (cardiac insufficiency) ở trẻ em, khi xuất hiện ở bệnh nhân lớn tuổi, tình trạng này có thể gây sa sút trí tuệ (dementia) và do đó cần phải can thiệp điều trị, với mục tiêu là làm giảm lưu lượng của luồng thông (shunt) động tĩnh mạch. Tình trạng ứ trệ tĩnh mạch (Venous congestion) do tăng lưu lượng dòng vào (input) (trong các tổn thương dạng rò) (Hình 13) hoặc giảm dòng chảy ra (outflow) (do hẹp thứ phát của kiểu dòng chảy ra) có thể liên quan đến suy giảm nhận thức hoặc động kinh (epilepsy); do đó, điều trị nhằm giảm lưu lượng luồng thông động tĩnh mạch là có giá trị.
Ngay cả khi không có các dấu hiệu ứ trệ tĩnh mạch, đường đi dài trên màng mềm của tĩnh mạch dẫn lưu có thể cho thấy tình trạng hạn chế dẫn lưu tĩnh mạch xuất hiện trên một diện rộng, làm tăng nguy cơ ứ trệ tĩnh mạch và động kinh sau đó. Ngược lại, tĩnh mạch ngắn dẫn lưu gần như trực tiếp vào xoang tĩnh mạch màng cứng (dural sinus) sẽ ít có khả năng gây cản trở việc dẫn lưu não bình thường. Nếu bệnh nhân có cấu trúc mạch máu dạng này mà vẫn bị động kinh, MRI cần được xem xét kỹ lưỡng (scrutinized) để tìm các dấu hiệu của tăng sinh tế bào thần kinh đệm quanh búi dị dạng nidus (perinidal gliosis).
Trong trường hợp thứ nhất (bệnh nhân động kinh có AVM với tĩnh mạch dẫn lưu màng mềm dài), can thiệp nội mạch được chỉ định nhằm giảm thiểu sự cản trở đối với quá trình dẫn lưu não bình thường, và có khả năng làm giảm tần suất hoặc mức độ nghiêm trọng của cơn co giật; trong trường hợp thứ hai (động kinh do tăng sinh tế bào thần kinh đệm quanh búi dị dạng nidus), can thiệp nội mạch ít có khả năng làm thay đổi tần suất hay mức độ nghiêm trọng của cơn co giật.
Hiệu ứng khối (Mass effect) là một cơ chế bệnh sinh (pathomechanism) hiếm gặp, có thể do các tĩnh mạch giãn lớn (venous ectasias) hoặc do sự chèn ép (compression) các cấu trúc quan trọng bởi chính búi dị dạng nidus; tình trạng này có thể dẫn đến động kinh, khiếm khuyết thần kinh, và thậm chí là não úng thủy. Hiện tượng ‘cướp máu động mạch – Arterial steal) có liên quan đến các dấu hiệu lâm sàng (ví dụ: đau đầu migraine và các triệu chứng thần kinh khu trú) thường có tính chất tạm thời. Với sự ra đời của các phương thức chẩn đoán hình ảnh mới như cộng hưởng từ chức năng (functional MRI) và cộng hưởng từ tưới máu (perfusion-weighted MRI), hiện nay có thể xác định liệu các triệu chứng của bệnh nhân có do hiện tượng cướp máu thực sự (true steal) gây ra hay không, và có thể được điều trị bằng phương pháp can thiệp nội mạch với mục đích giảm lưu lượng shunt nếu các triệu chứng gây tàn tật.
| Bảng 1
Các đặc điểm hình ảnh liên quan đến nguy cơ xuất huyết trong tương lai và khiếm khuyết thần kinh không do xuất huyết |
| Nguy cơ xuất huyết trong tương lai
– Tiền sử xuất huyết trước đó – Phình mạch trong búi dị dạng nidus – Hẹp hoặc giãn (dạng túi) tĩnh mạch – Dẫn lưu tĩnh mạch sâu – Dẫn lưu tĩnh mạch đơn độc – Vị trí ở hố sau hoặc nằm sâu |
| Nguy cơ khiếm khuyết thần kinh không do xuất huyết
– Luồng thông lưu lượng cao – Ứ trệ tĩnh mạch hoặc tắc nghẽn dòng chảy ra – Đường đi dài của tĩnh mạch dẫn lưu trên màng mềm – Tăng sinh tế bào thần kinh đệm xung quanh búi nidus – Hiệu ứng khối hoặc não úng thủy – Hiện tượng cướp máu động mạch. |
Hình 12. Dị dạng động tĩnh mạch (AVM) não vùng đồi thị, phân độ Spetzler-Martin độ 3, kèm theo phình mạch trong búi nidus (intranidal aneurysm) ở bé gái 4 tuổi nhập viện vì xuất huyết nội sọ tái phát. (a) Hình ảnh MRI xung T2W mặt phẳng axial cho thấy một búi mạch máu bất thường tại đồi thị trái, phù hợp với hình ảnh búi dị dạng nidus. Có một vùng xung quanh tăng tín hiệu trên T2 kèm viền giảm tín hiệu, các dấu hiệu này gợi ý tình trạng xuất huyết cũ trước đó. Cũng ghi nhận thêm một cấu trúc hình tròn trống tín hiệu của dòng chảy (flow void) ở mặt sau – bên của búi dị dạng nidus, có thể đại diện cho một túi phình trong búi nidus. (b) Hình ảnh chụp mạch động mạch đốt sống trái hướng nghiêng cho thấy nguồn cấp máu cho búi dị dạng nidus của AVM não đến từ các động mạch xuyên đồi thị (thalamoperforators) và các động mạch mạch mạc sau trái. Ghi nhận sự lấp đầy sớm của thuốc tương phản của túi phình nhỏ trong búi nidus (mũi tên).
Hình 13. Rò động tĩnh mạch màng mềm (Pial AVF) kèm theo các túi giãn tĩnh mạch và ứ trệ tĩnh mạch ở bé trai 7 tuổi nhập viện vì đau đầu. Bệnh nhân có tiền sử gia đình bị chảy máu mũi (nosebleeds) và giãn mao mạch niêm mạc (mucosal telangiectasias) gợi ý mắc bệnh giãn mao mạch xuất huyết di truyền (hereditary hemorrhagic telangiectasia). (a, b) Hình ảnh MRI xung T2W mặt phẳng axial (a) và hình ảnh cắt lớp vi tính mạch máu (CTA) mặt phẳng coronal (b) cho thấy các cấu trúc mạch máu giãn lớn ở vùng quanh rãnh Sylvius bên phải, gợi ý các túi giãn tĩnh mạch; kèm theo sự giãn lớn của động mạch não giữa (MCA) bên phải so với bên trái (mũi tên ở hình b) và không thấy búi dị dạng nidus rõ rệt. Các dấu hiệu này phù hợp với rò động tĩnh mạch màng mềm (Pial AVF). Tín hiệu cao (hyperintense) trên T2W của chất trắng tại thùy trán phải (mũi tên ở hình a) gợi ý tình trạng ứ trệ tĩnh mạch. (c) Hình ảnh chụp mạch động mạch cảnh trong phải hướng nghiêng cho thấy rò lưu lượng cao (high-flow fistula) giữa một nhánh của động mạch não giữa (MCA) và các túi giãn tĩnh mạch lớn.
Lựa chọn điều trị (Treatment Options)
Bên cạnh việc điều trị bảo tồn, có ba lựa chọn điều trị đối với AVM não: phẫu thuật (surgery), can thiệp thuyên tắc nội mạch (endovascular embolization), hoặc xạ phẫu (radiosurgery). Mỗi phương thức đều có những ưu điểm và nhược điểm riêng, và cách tiếp cận đa phương thức (multimodality approach) là phương pháp được sử dụng phổ biến nhất. Có các đặc điểm lâm sàng và hình ảnh học nhất định đóng vai trò quan trọng trong việc xác định phương pháp điều trị an toàn và hiệu quả nhất. Phẫu thuật có thể mang lại kết quả chữa trị nhanh chóng trong những trường hợp phù hợp; tuy nhiên, tỷ lệ biến chứng phụ thuộc phần lớn vào cấp độ Spetzler-Martin: cấp độ (grade) càng cao (hoặc càng thấp) thì tỷ lệ biến chứng càng cao (hoặc càng thấp). Do đó, những bệnh nhân có AVM não kích thước nhỏ hơn và nằm ở vỏ não thường là đối tượng được hưởng lợi nhiều nhất từ phương pháp phẫu thuật cắt bỏ (surgical resection) (Hình 14).
Can thiệp thuyên tắc nội mạch là lựa chọn điều trị khác có thể được sử dụng để nhanh chóng loại bỏ các yếu tố nguy cơ trên hình ảnh chụp mạch máu. Phương pháp can thiệp nội mạch này hầu như không có chống chỉ định (contraindications) thực sự; tuy nhiên, tỷ lệ chữa khỏi hoàn toàn (cure) nếu chỉ đơn thuần sử dụng thuyên tắc mạch (embolization) là tương đối thấp (khoảng 10%–20%), ngoại trừ các trường hợp rò động tĩnh mạch màng mềm (pial AVFs) lưu lượng cao hoặc các tổn thương kích thước nhỏ.
Bảng 2 tóm tắt các đặc điểm cấu trúc mạch máu có thể ít phù hợp hơn với can thiệp nội mạch và xạ phẫu. Xạ phẫu có tỷ lệ chữa khỏi cao với tỷ lệ biến chứng tương đối thấp. Tuy nhiên, hạn chế chính của phương pháp này là bức xạ (radiation) phát huy tác dụng chậm; có thể mất tới 2 năm trước khi ghi nhận bất kỳ sự co nhỏ nào của AVM não. Do đó, xạ phẫu có thể không phù hợp để điều trị AVM não có các yếu tố nguy cơ xuất huyết trong tương lai trên hình ảnh chụp mạch máu. Các tổn thương có thể tích lớn hơn 12 mL thường đi kèm với tỷ lệ chữa khỏi thấp hơn và tỷ lệ biến chứng cao hơn. Do những tác động của bức xạ, việc sử dụng xạ phẫu ở bệnh nhân nhi cần phải hết sức thận trọng.
Điều trị bảo tồn (Conservative management) thường được áp dụng khi nguy cơ từ việc điều trị là quá cao, như trong các trường hợp AVM não kích thước lớn hoặc ở những bệnh nhân không có triệu chứng và có nguy cơ xuất huyết thấp trong tương lai. Đối với các trường hợp AVM não kích thước lớn có kèm theo một hoặc nhiều yếu tố nguy cơ nói trên, phương pháp can thiệp thuyên tắc mạch trúng đích một phần (partial targeted embolization) đã được chứng minh là mang lại lợi ích trong việc ngăn ngừa xuất huyết trong tương lai.
Hình 14. Dị dạng động tĩnh mạch (AVM) não vùng thái dương, phân độ Spetzler-Martin grade 1 ở bé trai 15 tuổi, nhập viện vì đau đầu khởi phát đột ngột, sau đó là co giật. (a) Hình ảnh cắt lớp vi tính (CT scan) mặt phẳng axial cho thấy tổn thương tăng đậm độ kích thước nhỏ ở thùy thái dương phải, phù hợp với khối máu tụ trong nhu mô kích thước nhỏ. (b) Hình ảnh chụp mạch động mạch cảnh trong phải hướng nghiêng cho thấy AVM não kích thước nhỏ (< 3 cm), được cấp máu chủ yếu bởi các nhánh thái dương của động mạch não giữa (MCA) phải, với dẫn lưu tĩnh mạch nông đổ vào tĩnh mạch Labbe phải.
| Bảng 2
Các đặc điểm cấu trúc mạch máu kèm các nguy cơ liên quan trong điều trị can thiệp nội mạch hoặc xạ phẫu đối với dị dạng động tĩnh mạch (AVM) não |
||
| Đặc điểm cấu trúc mạch máu | Nguy cơ liên quan khi điều trị can thiệp nội mạch | Nguy cơ liên quan khi điều trị xạ phẫu |
| 1. Động mạch: | ||
| – Phình mạch liên quan đến dòng chảy | – Nguy cơ xuất huyết trong quá trình can thiệp cao hơn | … |
| – Các mạch máu nuôi động mạch gián tiếp (động mạch kiểu đi qua – passage type) | – Khoảng cách an toàn ngắn đối với dòng trào ngược | … |
| – Nhiều động mạch nuôi nhỏ | – Cơ hội thấp đối với việc điều trị khỏi hoàn toàn. | … |
| 2. Nidus: | ||
| – Có nhiều ngăn nhỏ | – Cơ hội thấp đối với việc điều trị khỏi. | … |
| – Kích thước lớn hơn 12mL | … | – Cơ hội thấp đối với việc điều trị khỏi. |
| 3. Tĩnh mạch: | ||
| – Hẹp tĩnh mạch | – Nguy cơ biến chứng cao hơn nếu trôi vật liệu thuyên tắc mạch. | … |
| 4. Khác: | ||
| – Bệnh nhân trẻ tuổi | … | – Tăng nguy cơ xuất hiện AVM não nguy cơ cao thứ phát. |
| – Các yếu tố nguy cơ xuất huyết trong tương lai (xem bảng 1) | … | – Có thể xuất huyết do bức xạ tác động. |
Tóm tắt
Chúng tôi đã mô tả các đặc điểm hình ảnh điển hình của AVM não, cũng như các tổn thương mạch máu não có đặc điểm tương tự (mimics) với AVM não. Vì diễn tiến tự nhiên và các lựa chọn điều trị của những tổn thương ‘giả AVM’ này rất khác biệt, nên việc bác sĩ chẩn đoán hình ảnh có khả năng phân biệt chúng với AVM não điển hình là điều vô cùng quan trọng. Ngoài ra, chúng tôi đã thảo luận về những câu hỏi quan trọng nhất cần được trả lời khi bác sĩ chẩn đoán hình ảnh gặp AVM não, bao gồm việc liệu có sự hiện diện của các yếu tố nguy cơ gây xuất huyết trong tương lai hoặc các khiếm khuyết thần kinh không do xuất huyết hay không.
Chúng tôi cũng đã mô tả các đặc điểm hình ảnh có thể giúp dự đoán những nguy cơ liên quan đến từng lựa chọn điều trị, từ đó giúp các bác sĩ lâm sàng đưa ra quyết định phù hợp trong việc quản lý điều trị những tổn thương này.
Tài liệu tham khảo
Radiologic Assessment of Brain Arteriovenous Malformations: What Clinicians Need to Know
Người dịch: Bs. Lê Thị Ny Ny – Radiology
Để lại một phản hồi Hủy