1. U nguyên bào thần kinh đệm đa hình (Glioblastoma Multiforme)
*Dấu hiệu hình ảnh đặc hiệu (Specific Imaging Findings)
U nguyên bào thần kinh đệm đa hình (GBM) thường biểu hiện dưới dạng khối u bắt thuốc không đồng nhất. GBM thường giảm đậm độ trên CT và có tín hiệu cao trên xung T2W MRI. Vùng tín hiệu cao trên T2W hoặc giảm đậm độ trên CT kèm phù mạch (vasogenic edema) xung quanh tổn thương là hầu như luôn bắt thuốc, nhưng kích thước của tổn thương thì thay đổi.
Đặc điểm của u thần kinh đệm (gliomas) là phù thâm nhiễm (infiltrative edema) với bất thường tín hiệu không chỉ giới hạn ở chất trắng mà còn lan rộng đến cả vỏ não và/hoặc chất xám sâu (deep gray matter). Đặc điểm này hầu như luôn xuất hiện cùng với ít nhất một phần của vùng bất thường. Mặc dù tụ máu rõ rệt trong u (frank intratumoral hematomas) là không thường gặp, nhưng nhiều vùng tín hiệu thấp đen do hiệu ứng thuận từ của một lượng nhỏ sản phẩm máu hầu như luôn được phát hiện trên xung T2* MRI.
Xung T1W có tiêm Gadolinium thường cho thấy khối u hoại tử (necrotic mass) kèm bắt thuốc mạnh, không đều, chủ yếu ở ngoại vi. Bắt thuốc dạng nốt (Nodular) hoặc dạng vòng (ring-like) cũng có thể có, và trong một số trường hợp hiếm gặp thì khối u không bắt thuốc. Phần đặc của khối u thường có hạn chế khuếch tán (low diffusion) với giá trị ADC thấp, trong khi các vùng hoại tử thì sáng trên bản đồ ADC. Trên MRI phổ (MRS) sẽ thấy choline tăng, NAA giảm và đỉnh lactate/lipid tăng cao.
Thể tích máu não vùng tương đối (rCBV) rất cao ở các vùng khối u đặc là một dấu hiệu điển hình của GBM trên các hình ảnh tưới máu. Phân tích đường cong tín hiệu trên các hình ảnh tưới máu nhạy từ sau tiêm thuốc tương phản (susceptibility-weighted post-contrast perfusion studies) cho thấy tín hiệu trở về giá trị cơ bản sau lần tiêm thuốc tương phản đầu tiên. Trong khoảng 10% trường hợp, GBM biểu hiện dưới dạng các tổn thương đa ổ trên hình ảnh ban đầu.
*Thông tin lâm sàng liên quan (Pertinent Clinical Information)
Bệnh nhân có thể biểu hiện khiếm khuyết thần kinh khu trú (focal neurological deficits) hoặc các dấu hiệu tăng áp lực nội sọ. Co giật ít gặp hơn lúc chẩn đoán so với u thần kinh đệm độ thấp (low-grade gliomas). GBM thường xuất phát ở bán cầu đại não và độ tuổi khởi phát cao nhất là thập kỷ thứ sáu hoặc thứ bảy của cuộc đời (50 – 70 tuổi).
*Chẩn đoán phân biệt
– Khối u di căn (Metastatic Tumor)
+ Phù mạch rõ rệt, không có phù thâm nhiễm
+ Kết quả phổ bình thường bên ngoài vùng bắt thuốc trên MRI phổ
+ Trên hình ảnh tưới máu, tín hiệu không trở về mức cơ bản (baseline)
+ Các vùng tín hiệu thấp đen do hiệu ứng nhạy từ (susceptibility effects) trên xung T2* là rất ít và kín đáo.
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Tổn thương là đồng nhất và không có hoại tử, ngoại trừ ở bệnh nhân dương tính với HIV
+ Rất hạn chế khuếch tán (very low diffusion), tối trên bản đồ ADC
+ Không có vùng tín hiệu thấp đen do hiệu ứng nhạy từ trên xung T2*
+ Phù mạch rõ rệt.
– Tổn thương hủy myelin dạng tạo khối (Tumefactive Demyelinating Lesion – TDL)
+ Thường có bắt thuốc dạng vòng không hoàn toàn
+ Thể tích máu não vùng tương đối (rCBV) thấp trên hình ảnh tưới máu.
– Áp xe (Abscess)
+ Có hạn chế khuếch tán ở lõi hoại tử (necrotic core) với tín hiệu sáng trên DWI và giá trị ADC thấp.
– Nhồi máu não giai đoạn bán cấp (Subacute Infarction)
+ Bắt thuốc dạng hồi não (gyriform enhancement) là thường gặp
+ Tổn thương theo vùng phân bố mạch máu
+ rCBV rất thấp trên hình ảnh tưới máu
+ Thường có tín hiệu đồng nhất khắp tổn thương, trừ khi có xuất huyết.
*Kết luận
U nguyên bào thần kinh đệm đa hình (GBM) là u thần kinh đệm (glioma) ác tính thường gặp nhất ở người lớn. Theo phân loại khối u hệ thần kinh trung ương của WHO, GBM có thêm 2 biến thể: u nguyên bào thần kinh đệm tế bào khổng lồ (giant cell glioblastoma) và sarcoma thần kinh đệm (gliosarcoma), và tất cả đều là khối u độ IV (grade IV neoplasm). Các tế bào u được tìm thấy bên ngoài vùng bất thường tín hiệu trên MRI, vì vùng quanh u bị thâm nhiễm bởi các tế bào ác tính. Cũng có bằng chứng cho thấy sự thâm nhiễm của các tế bào u hiện diện ở cả bán cầu não đối bên ngay cả với những khối u mới được chẩn đoán ở bệnh nhân chưa điều trị, và GBM nên được coi là bệnh lý của toàn bộ não.
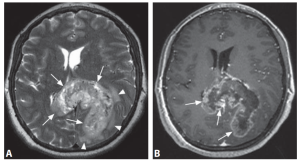
Hình 1. GBM: Hình ảnh trên xung T2W axial (A) cho thấy một khối u lớn không đồng nhất (các mũi tên) xuất phát ở lồi thể chai (splenium of the corpus callosum) và xâm lấn vào cả hai bán cầu đại não, kèm chèn ép não thất. Ghi nhận vùng phù quanh u tương đối ít (các đầu mũi tên). Khối u này cho thấy bắt thuốc mạnh không đồng nhất, chủ yếu ở ngoại vi (các mũi tên) trên xung T1W sau tiêm thuốc tương phản (B).
Hình 2. GBM: Xung FLAIR (A) cho thấy một khối u trong trục (mũi tên đen) kèm phù mạch (vasogenic edema) xung quanh (các đầu mũi tên). Ngoài ra còn có phù thâm nhiễm (infiltrative edema) kèm xâm lấn vỏ não (mũi tên trắng). Các vùng có tín hiệu thấp bên trong (các đầu mũi tên) trên xung T2* SWI (B). Thể tích máu não vùng tương đối (rCBV) là cao nằm dọc theo ngoại vi của tổn thương (các mũi tên) trong khi rCBV thấp ở vùng hoại tử trung tâm (*) trên hình ảnh MRI tưới máu (C).
Hình 3. GBM: Hình ảnh thể tích máu não (CBV) trên CT tưới máu (CT perfusion) (A) ở bệnh nhân bị liệt nửa người bên phải và rối loạn ngôn ngữ (dysphasia) (nghi ngờ nhồi máu não cấp) cho thấy một vùng vỏ não – dưới vỏ ở thùy trán trái có CBV rất cao (mũi tên) và một vùng khu trú ở chất trắng tăng tưới máu (hyperperfusion) (đầu mũi tên). Hình ảnh trên T1W coronal sau tiêm thuốc tương phản (B) cho thấy cả hai tổn thương đều bắt thuốc (các mũi tên). Xung FLAIR (C) ở cùng mức lát cắt với hình A cho thấy các khối này tăng tín hiệu (các mũi tên). Tăng tín hiệu bất thường này lan rộng đến vỏ não (các đầu mũi tên), phù hợp với phù thâm nhiễm.
2. Hoại tử não do điều trị (Therapy-Induced Cerebral Necrosis) (Hoại tử não do xạ trị – Radiation Necrosis)
*Dấu hiệu hình ảnh đặc hiệu (Specific Imaging Findings)
Hoại tử não do điều trị (xạ trị) (Therapy-induced cerebral necrosis – TCN) không thể phân biệt một cách đáng tin cậy với khối u ác tính còn lại (residual)/tiến triển (progressive) trên hình ảnh CT hoặc MRI thông thường. Hoại tử não do xạ trị (TCN) biểu hiện dưới dạng khối u bắt thuốc kèm phù mạch xung quanh, thường tăng kích thước trên các phim chụp theo dõi. Có thể thấy các vùng dạng đường không đều bên trong có tín hiệu cao trên T1W.
Các kiểu bắt thuốc tương phản điển hình bao gồm các đốm khu trú (localized specks) bắt thuốc có tín hiệu cao bên trong các vùng hoại tử (“phô mai Thụy Sĩ (Swiss cheese)/bong bóng xà phòng (soap bubble)” – có thể là do thuốc tương phản rò rỉ vào các khoang nhỏ bên trong mô hoại tử) và bắt thuốc ở ngoại vi dạng lông chim (feathery) có giới hạn không rõ (“mặt sóng lan truyền – spreading wavefront”). Phù (Edema) chỉ giới hạn ở chất trắng mà không xâm lấn thâm nhiễm vào chất xám. Trên hình ảnh tưới máu, hoại tử não do xạ trị (TCN) có đặc trưng là thể tích máu não tương đối (rCBV) rất thấp, trái ngược với các khối u ác tính.
Đường cong tín hiệu – thời gian của hình ảnh tưới máu cho thấy khả năng phục hồi tín hiệu thấp hơn đáng kể so với ở u thần kinh đệm (gliomas) cho thấy mức độ rò rỉ thuốc tương phản cao bên trong hoại tử não do xạ trị (TCN). Vùng hoại tử có tín hiệu cao trên bản đồ ADC, so với giá trị ADC tương đối thấp của các khối u còn hoạt tính (viable neoplasms). Hoại tử não do xạ trị (TCN) được đặc trưng bởi sự giảm tất cả các chất chuyển hóa trên hình ảnh MRI phổ và nồng độ lipid rất cao chiếm ưu thế, được gọi là “đỉnh tử thần – death peak”.
*Thông tin lâm sàng liên quan
Hoại tử não do xạ trị (TCN) là một biến chứng nghiêm trọng của liệu pháp xạ trị cho các khối u nội sọ (intracranial tumors) và các tổn thương không phải khối u (non-neoplastic conditions). Hoại tử não do xạ trị cũng xảy ra sau khi điều trị các bệnh lý ngoài sọ (extracranial diseases), đặc biệt là ung thư biểu mô vòm họng (hầu mũi) (nasopharyngeal carcinoma). Sự phát triển của hoại tử não do xạ trị (TCN) có liên quan đến phương pháp truyền bức xạ, tổng liều, kích thước phân liều (liều lượng mỗi lần xạ trị), thể tích điều trị, tuổi của bệnh nhân và việc sử dụng hóa trị. Các thay đổi trên não xảy ra từ vài tháng đến vài năm sau điều trị, thường xảy ra hơn sau khi xạ trị tại chỗ liều cao như phẫu thuật xạ trị (radiosurgery) hoặc xạ trị áp sát (brachytherapy).
Xạ trị (Radiation therapy) kết hợp với temozolomide, đặc biệt trong 3 tháng đầu, thường dẫn đến hoại tử não do xạ trị (TCN) ở những bệnh nhân bị u não nguyên phát (primary brain tumors), được gọi là giả tiến triển (pseudoprogression). Điều trị chuẩn bao gồm phẫu thuật cắt bỏ (surgical resection) cũng giúp xác định chẩn đoán, và dùng corticosteroid. Liệu pháp chống tạo mạch máu (Antiangiogenic therapy) với bevazucimab gần đây đã cho thấy kết quả tuyệt vời ở những bệnh nhân bị hoại tử não do xạ trị (TCN).
*Chẩn đoán phân biệt
– U thần kinh đệm độ cao tiến triển (Progressive High-Grade Glioma)
+ Thể tích máu não (CBV) tăng trên hình ảnh tưới máu
+ Tỷ lệ Cho/NAA và Cho/Cr tăng cao trên MRI phổ (MRS)
+ Giá trị ADC thấp ở thành phần đặc của u
– Áp xe (Abscess)
+ Bắt thuốc viền với bờ đều (smooth rim of enhancement) mà không có các ổ bắt thuốc bên trong
+ Phần trung tâm không bắt thuốc có tín hiệu rất sáng trên DWI và rất thấp trên ADC
+ Viền ngoại vi có tín hiệu thấp trên T2 và tín hiệu cao trên T1
– Khối u di căn (Metastatic Neoplasm)
+ Thể tích máu não (CBV) tăng trên hình ảnh tưới máu
+ Tăng Cho, không có bằng chứng của NAA trên MRI phổ (MRS)
+ Thường có hình dạng tròn và giới hạn rõ.
*Kết luận
Hoại tử não do điều trị (TCN) trước đây được gọi là hoại tử do xạ trị (radiation necrosis); tuy nhiên, các liệu pháp chống ung thư bổ sung (additional antineoplastic therapies) thường góp phần gây tổn thương mô do bức xạ. Một số cơ chế có thể liên quan đến sinh bệnh học (pathogenesis); tuy nhiên, tổn thương vi mạch máu não (brain microvasculature) có thể là nguyên nhân chính dẫn đến sự phát triển tổn thương não. Chết tế bào nội mô (Endothelial cell death) dẫn đến phá vỡ hàng rào máu não (blood–brain barrier), phù và thiếu oxy.
Thiếu oxy (Hypoxia) được cho là gây ra sự điều hòa tăng cường yếu tố tăng trưởng nội mô mạch máu, làm tăng tính thấm của mạch máu (permeability of the vasculature) gây phù mạch, huyết khối mạch máu và hoại tử mô. Về mặt mô học, các tổn thương hoại tử khu trú cho thấy những thay đổi mạch máu điển hình bao gồm tình trạng hyalin hóa, hoại tử dạng fibrin (fibrinoid necrosis) của thành mạch máu và lòng mạch bị hẹp. Chất trắng ở rìa tổn thương có thể cho thấy mất myelin và tăng sinh thần kinh đệm dạng hình sao (astrocytic gliosis), trong khi hoại tử đông (coagulative necrosis) hiện diện ở vùng trung tâm.
U thần kinh đệm (glioma) tiến triển và hoại tử não do xạ trị thường cùng tồn tại, và u còn sót lại (residual tumor foci) thường vẫn hiện diện ngay cả trong trường hợp được gọi là hoại tử do xạ trị đơn thuần (pure radiation necrosis). Các nghiên cứu gần đây cho thấy sự phân biệt đáng tin cậy giữa hoại tử não do xạ trị và u di căn còn hoạt tính bằng FDG-PET/CT hai thì (dual phase) bằng cách sử dụng sự thay đổi của tỷ lệ SUVmax (Giá trị hấp thụ chuẩn tối đa (Maximum Standardized Uptake Value)) giữa tổn thương và chất xám theo chức năng thời gian.
Hình 1. Hoại tử não do xạ trị (TCN): Hình ảnh trên T1W sau tiêm thuốc tương phản (A) sau khi điều trị u thần kinh đệm độ cao (high-grade glioma) cho thấy tổn thương dạng khối bắt thuốc với các đốm bắt thuốc tương phản bên trong và viền có giới hạn không rõ (các mũi tên). Hình ảnh MRI tưới máu tương ứng (B) không cho thấy bất kỳ sự tăng rCBV nào (các mũi tên).
Hình 2. Hoại tử não do xạ trị: Hình ảnh trên T1W sau tiêm thuốc tương phản ở u màng não (meningioma) đã điều trị cho thấy một tổn thương trong trục (intra-axial lesion) băng qua đường giữa với các đốm bắt thuốc bên trong (các đầu mũi tên) và bờ ngoài cùng dạng lông chim với giới hạn không rõ (các mũi tên).
Hình 3. Hoại tử não do xạ trị: Hình ảnh trên FLAIR axial sau khi điều trị u thần kinh đệm độ cao (high-grade glioma) cho thấy một tổn thương dạng khối ở thùy trán trái (*) băng qua đường giữa với phù mạch xung quanh (các đầu mũi tên). Hình ảnh PET axial được tích hợp (coregistered) với MRI T1W sau tiêm thuốc tương phản (B) cho thấy giảm hoạt động chuyển hóa ở thùy trán trái và sự hấp thu FDG thấp hơn ở phần bắt thuốc của tổn thương (mũi tên) so với vỏ não đối bên (contralateral cortex). Ghi nhận các ổ bắt thuốc bên trong (các đầu mũi tên).
Hình 4. Hoại tử não do xạ trị: Hình ảnh trên xung FLAIR axial (A) của u schwannoma của dây thần kinh tiền đình (dây thần kinh số VIII) (vestibular schwannoma) (*) đã được điều trị bằng phẫu thuật (surgery) và phẫu thuật xạ trị (radiosurgery) cho thấy một tổn thương choán chỗ (mass effect) (*) có tăng tín hiệu xung quanh (các mũi tên). Hình ảnh T1W sau tiêm thuốc tương phản (B) cho thấy bắt thuốc tương phản dạng đốm ở trung tâm và dạng lông chim ở ngoại vi (các mũi tên) xung quanh khối u (đầu mũi tên). Ghi nhận kiểu bắt thuốc bên trong (internal enhancement pattern) tương tự khối u đã được điều trị.
Hình 5. Hoại tử não do xạ trị: Hiệu ứng khối (mass effect) và phù ở thùy trán phải (các đầu mũi tên) bao quanh một vùng có tín hiệu cao không đều trên T1W (các mũi tên) (A), vùng này cho thấy bắt thuốc tương phản ở ngoại vi có giới hạn không rõ (các mũi tên) và bắt thuốc rải rác bên trong (đầu mũi tên) (B).
3. Di căn não không xuất huyết (Non-Hemorrhagic Metastases)
*Dấu hiệu hình ảnh đặc hiệu (Specific Imaging Findings)
Các khối u di căn (Metastatic neoplasms) đến não có thể xuất hiện ở bất cứ đâu; tuy nhiên, hầu hết được tìm thấy ở ranh giới chất xám – chất trắng ngoại vi trên lều tiểu não (supratentorial peripheral gray–white matter junction), tiếp theo là ở tiểu não (cerebellum) và hạch nền (basal ganglia). Tổn thương là các khối riêng biệt, đa ổ hoặc đơn ổ, với mức độ phù mạch khác nhau ở chất trắng xung quanh. Phù và hiệu ứng khối thường rất nổi trội (prominent) và không tương xứng với kích thước của tổn thương, ngoại trừ các khối u di căn ở vỏ não và các khối u di căn có kích thước rất nhỏ thì gây phù xung quanh rất ít.
Phần lớn các khối u có đậm độ thấp (hypodense) trên CT và tín hiệu thấp trên T1 MRI. Các khối u có tỷ lệ nhân/tế bào chất cao hoặc chứa chất nhầy, như ung thư biểu mô tuyến (adenocarcinomas) có đậm độ cao trên CT. Các khối u hoại tử và dạng nang có tín hiệu cao trên T2. Các khối u có mật độ tế bào cao cho thấy đồng tín hiệu đến tín hiệu thấp, trong khi thành phần nhầy và vôi hóa cho tín hiệu rất thấp trên T2 thường thấy ở ung thư biểu mô tuyến (adenocarcinomas). Các khối u di căn không xuất huyết luôn bắt thuốc tương phản theo kiểu dạng nốt hoặc dạng vòng, điển hình với bờ không đều nhưng sắc nét.
Hình ảnh xung T1W 3D (Volumetric T1WI) cải thiện khả năng phát hiện các ổ tổn thương nhỏ (punctate deposits) mà không có phù. Các khối u di căn cho thấy đặc điểm khuếch tán MRI thay đổi. Tuy nhiên, phần trung tâm của tổn thương bắt thuốc dạng vòng thường tối trên DWI và sáng trên bản đồ ADC, phù hợp với độ khuếch tán cao (high diffusivity), chỉ có một số trường hợp ngoại lệ rất hiếm là có hạn chế khuếch tán. Hình ảnh tưới máu cho thấy thể tích máu não vùng tương đối (rCBV) tăng lên của khối u bắt thuốc, với sự phục hồi tín hiệu chậm trên đường cong tín hiệu – thời gian, trái ngược với mô não bình thường và u thần kinh đệm (gilomas). MRI phổ (MRS) cho thấy nồng độ choline tăng và nồng độ NAA giảm một cách không đặc hiệu. Cả MRS và rCBV về cơ bản đều bình thường ở vùng phù kế cận không bắt thuốc.
*Thông tin lâm sàng liên quan
Các triệu chứng không đặc hiệu và tiến triển, bao gồm đau đầu, khiếm khuyết thần kinh khu trú, co giật, buồn nôn, nôn và thay đổi ý thức. Điều trị bao gồm điều trị triệu chứng và xạ trị toàn bộ não (WBRT – whole-brain radiation), cùng với phẫu thuật (surgery) (đối với một đến một vài tổn thương) hoặc phẫu thuật xạ trị (radiosurgery) (đối với các tổn thương có kích thước nhỏ hơn). Kiểm soát khối u toàn thân, số lượng và vị trí của các tổn thương não, cùng với tuổi và tình trạng thể chất của bệnh nhân là các yếu tố tiên lượng quan trọng.
*Chẩn đoán phân biệt
– U thần kinh đệm độ cao (High-Grade Glioma)
+ Bắt thuốc tương phản có giới hạn kém rõ, có thể có các phần đặc không bắt thuốc
+ Phù thâm nhiễm xung quanh vùng bắt thuốc lan vào chất xám
+ Vùng phù không bắt thuốc cho thấy rCBV tăng trên hình ảnh tưới máu
+ Vùng phù không bắt thuốc cho thấy nồng độ choline cao và NAA thấp trên MRI phổ
+ Thường là tổn thương chất trắng sâu.
– Áp xe (Abscess)
+ Tín hiệu sáng chói như “bóng đèn – light bulb” ở trung tâm trên DWI
+ Bắt thuốc viền mỏng và đều
+ Viền tổn thương có tín hiệu thấp trên T2 và tín hiệu cao trên T1
+ rCBV không tăng trên hình ảnh tưới máu
– Hủy myelin dạng tạo khối (Tumefactive Demyelination)
+ Không có hoặc có phù mạch nhẹ và hiệu ứng khối rất nhẹ (minimal mass effect)
+ Đặc trưng với bắt thuốc dạng vòng không hoàn toàn ở các tổn thương lớn
+ rCBV không tăng trên hình ảnh tưới máu
+ Tổn thương không bắt thuốc là rất thường gặp.
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Thường là tổn thương nằm sâu, không phải ở ngoại vi
+ Tín hiệu thấp đồng nhất trên bản đồ ADC
+ Bắt thuốc mạnh đồng nhất điển hình.
*Kết luận
Khoảng 10% bệnh nhân ung thư phát triển di căn não (brain metastases) và trong một số trường hợp thì di căn não là nguyên nhân gây ra các triệu chứng ban đầu. Tỷ lệ di căn não dường như đang gia tăng, làm hạn chế những lợi ích đạt được từ các phương pháp điều trị toàn thân mới. Não được coi là một “vị trí trú ẩn – sanctuary site” vì hàng rào máu – khối u làm hạn chế khả năng thuốc đi vào và tiêu diệt các tế bào ác tính. Các tác dụng phụ nghiêm trọng của xạ trị toàn bộ não (WBRT) cùng với những hiệu quả gần đây trong điều trị tại chỗ (local control) và tỷ lệ sống còn đã dẫn đến việc xem xét lại vai trò của xạ trị toàn bộ não (WBRT) phương pháp mà có thể không mang lại lợi ích cho tất cả bệnh nhân.
Hình 1. Di căn não: Hình ảnh CT sau tiêm thuốc tương phản (1A) cho thấy nhiều tổn thương ở não bắt thuốc (các mũi tên trắng) với phù mạch đậm độ thấp xung quanh (các đầu mũi tên đen). Có thêm các khối u ở tiểu não hai bên (1B).
Hình 2. Di căn não: Hình ảnh CT không tiêm thuốc tương phản (2A) cho thấy phù mạch đối xứng hai bên (các đầu mũi tên đen) ở hai bán cầu đại não phía sau. Hình ảnh sau tiêm thuốc tương phản (2B) cho thấy một tổn thương hình bầu dục (mũi tên) có viền bắt thuốc không đều.
Hình 3. Di căn não: Hình ảnh trên FLAIR axial ở bệnh nhân bị ung thư phổi (A) cho thấy 2 vùng phù (các mũi tên) chứa các tổn thương bắt thuốc dạng viền được thấy trên xung T1W sau tiêm thuốc tương phản (B). Hình B: Một tổn thương có viền mỏng, đều (mũi tên), trong khi tổn thương còn lại cho thấy sự bắt thuốc ngoại vi không đều và bắt thuốc nhẹ không đồng nhất bên trong (đầu mũi tên). Xung DWI tương ứng (C) cho thấy tín hiệu thấp ở trung tâm của cả hai tổn thương (các mũi tên).
Hình 4. Di căn não: Hình ảnh trên T2W (A) ở bệnh nhân ung thư vú cho thấy các khối u có tín hiệu thấp (các mũi tên) kèm phù xung quanh. Sự bắt thuốc của tổn thương chủ yếu ở ngoại vi được thấy trên xung T1W sau tiêm thuốc tương phản (B).
Hình 5. Di căn não: Hình ảnh T1W sau tiêm thuốc tương phản sagittal (A) cho thấy một ổ nhỏ bắt thuốc ban đầu bị bỏ sót (mũi tên) ở hồi sau trung tâm (post-central gyrus) bên phải, cũng được thấy trên mặt phẳng axial (B). Hình ảnh sau tiêm thuốc tương phản mặt phẳng sagittal theo dõi (C) cho thấy tổn thương tăng kích thước đáng kể. Bắt thuốc viền dạng nốt một phần được bao quanh bởi phù mạch (đầu mũi tên). Tín hiệu rất thấp hiện diện ở phần trung tâm không bắt thuốc (mũi tên) trên DWI (D).
4. Áp xe não (Cerebral Abscess)
*Dấu hiệu hình ảnh đặc hiệu (Specific Imaging Findings)
Áp xe não (Cerebral abscess) có thể xảy ra ở bất kỳ vị trí nào của não, nhưng có xu hướng nằm ở ranh giới chất xám – chất trắng trên lều tiểu não của thùy trán và thùy đỉnh. Trên CT, áp xe não thường biểu hiện dưới dạng một vùng dưới vỏ có phù mạch giảm đậm độ đáng kể với hiệu ứng khối và một tổn thương dạng hình tròn ở trung tâm có đậm độ thấp hơn, đôi khi có viền mỏng đồng đậm độ, viền này sẽ bắt thuốc trên hình ảnh sau tiêm thuốc tương phản.
Phần trung tâm của áp xe có tín hiệu thấp trên T1 và tín hiệu cao trên T2 (hơi cao hơn dịch não tủy). Vỏ bao (capsule) có đặc điểm là tín hiệu cao trên T1 và tín hiệu thấp trên T2 kèm bắt thuốc tương phản mạnh. Viền bắt thuốc nhìn chung là mỏng và đều, đặc biệt ở phía ngoài cùng. Áp xe có xu hướng lan rộng vào đường giữa và trở thành hình bầu dục, do đó vỏ bao của áp xe có thể mỏng hơn ở phía não thất và dày hơn ở phía vỏ não.
Chụp MRI khuếch tán (Diffusion MR imaging) là kỹ thuật chẩn đoán hình ảnh chính xác nhất để phân biệt áp xe do vi khuẩn (bacterial abscess) với các khối u dạng nang/hoại tử trong sọ khác. Ngoài có tín hiệu cao trên FLAIR và T1W thì phần trung tâm của áp xe có tín hiệu rất sáng trên DWI và tối tương ứng trên ADC, cho thấy có hạn chế khuếch tán bên trong dịch mủ (purulent material). Áp xe do nấm (Fungal abscesses) có thể không đồng nhất hơn, cho thấy giá trị ADC cao hơn, và có thể ảnh hưởng đến chất xám sâu.
Hình ảnh MRI phổ (MRS) cho thấy dạng phổ phức tạp (complex spectra) bên trong ổ áp xe với nhiều đỉnh bất thường bao gồm lactate và lipid, cũng như acetate, succinate và axit amin. Hình ảnh tưới máu tương tự như các quá trình viêm và nhiễm trùng khác, thường cho thấy thể tích máu não giảm đến bình thường.
*Thông tin lâm sàng liên quan
Áp xe là bệnh lý có khả năng gây tử vong nhưng dễ điều trị. Triệu chứng lâm sàng phổ biến nhất là đau đầu, tiếp theo là sốt, thay đổi trạng thái tinh thần, khiếm khuyết thần kinh khu trú và co giật. Tiên lượng phụ thuộc vào kích thước và vị trí của ổ áp xe, độc lực (virulence) của vi sinh vật, và tình trạng miễn dịch của bệnh nhân. Các biến chứng bao gồm vỡ vào não thất gây viêm não thất (ventriculitis) có tỷ lệ tử vong cao và thoát vị não do hiệu ứng khối. Điều trị bao gồm phẫu thuật dẫn lưu (surgical drainage) hoặc phẫu thuật cắt bỏ (surgical excision) và dùng kháng sinh đường tĩnh mạch.
*Chẩn đoán phân biệt
– Khối u hoại tử (Necrotic Neoplasm) (nguyên phát (primary) hoặc thường gặp hơn là di căn (metastatic))
+ Phần trung tâm của tổn thương bắt thuốc dạng viền có tín hiệu thấp trên DWI và sáng trên bản đồ ADC
+ Viền bắt thuốc thường dày không đều với đường bờ tạo nốt
+ Viền có tín hiệu thấp trên T2 là hiếm gặp.
– Hủy myelin dạng tạo khối (Tumefactive Demyelination)
+ Phù mạch và hiệu ứng khối là không có hoặc có rất nhẹ.
+ Bắt thuốc ở ngoại vi dạng vòng không hoàn toàn
– Khối máu tụ giai đoạn bán cấp (Subacute Hematoma)
+ Hiện diện các sản phẩm của máu
+ Bắt thuốc ở ngoại vi mỏng, không đều hoặc đa cung.
– Bệnh nhiễm ấu trùng sán dây lợn ở não (Neurocysticercosis) (giai đoạn tạo keo (colloidal) và giai đoạn tạo mô hạt (granular))
+ Thường không có tín hiệu sáng trên DWI
+ Phù mạch thường nhẹ
+ Có thể có các tổn thương vôi hóa
*Kết luận
Áp xe được gây ra do các tác nhân gây bệnh (pathogens) xâm nhập vào hệ thần kinh trung ương (CNS) bằng cách lây lan theo đường máu (hematogenous spread) trong trường hợp nhiễm trùng huyết (sepsis) hoặc từ ổ nhiễm trùng ở xa, lan rộng từ ổ nhiễm trùng kế cận, hoặc đi vào qua vết thương trong chấn thương (bao gồm cả phẫu thuật). Nhìn chung, vi sinh vật phổ biến nhất là liên cầu khuẩn (Streptococcus); tuy nhiên, nhiều loại vi khuẩn khác cũng có thể liên quan, và tác nhân gây bệnh có mối liên hệ chặt chẽ với tuổi và tình trạng toàn thân của bệnh nhân.
Áp xe tiến triển từ viêm não (cerebritis) thành áp xe não trưởng thành (mature abscess) thường trong vòng 2 – 3 tuần. Tổn thương vi mạch máu do vi khuẩn gây ra dẫn đến viêm khu trú (local inflammation), xuất huyết lấm tấm (petechial hemorrhage), dịch xuất tiết chứa fibrin quanh mạch máu (perivascular fibrinous exudates), phù và hoại tử nhu mô não. Theo thời gian, dịch mủ (purulent material) kết lại và được bao quanh bởi mô hạt viêm (inflammatory granulation tissue) và vỏ bao collagen.
MRI phổ (MRS) có thể giúp phân biệt các loại áp xe do vi khuẩn hiếu khí (aerobic), kỵ khí (anaerobic), do nấm (fungal) và lao (TB). Mặc dù sự bắt thuốc tương phản còn lại (residual contrast enhancement) có thể kéo dài hàng tháng sau khi điều trị thành công, nhưng sự giảm tín hiệu thấp của vỏ bao trên T2 (decreasing T2 hypointensity of the capsule) và sự co lại (shrinkage) của trung tâm hoại tử xảy ra sớm hơn và là những dấu hiệu đáng tin cậy hơn của quá trình hồi phục. Tín hiệu cao kéo dài hoặc xuất hiện lại trên DWI và giá trị ADC thấp cho thấy thất bại của điều trị.
Hình 1. Áp xe não: Xung FLAIR axial (A) cho thấy một vùng tín hiệu cao không đều (patchy) (các mũi tên trắng) ở vùng dưới vỏ thùy đỉnh trái kèm một tổn thương hình bầu dục bên trong có giới hạn rõ bởi một viền giảm tín hiệu sắc nét (đầu mũi tên đen). Xung T1W sau tiêm thuốc tương phản tương ứng (B) cho thấy bắt thuốc dạng vòng rõ rệt (marked ring-like enhancement) của viền tổn thương (mũi tên) và một tổn thương bắt thuốc khác (đầu mũi tên). Xung DWI (C) cho thấy thành phần bên trong có tín hiệu rất sáng (mũi tên) và trên bản đồ ADC (D) thì rất tối (mũi tên), phù hợp với có hạn chế khuếch tán (reduced diffusivity). Phù mạch kèm theo có tăng khả năng khuếch tán (increased diffusivity) (các đầu mũi tên).
Hình 2. Áp xe não: Hình CT không tiêm thuốc tương phản mặt phẳng axial ở bệnh nhân bị đau đầu, co giật và sốt sau khi phẫu thuật mở sọ thái dương (temporal craniotomy) bên trái gần đây cho thấy phù mạch giảm đậm độ (các mũi tên) ở vùng não bên dưới với một vùng giảm đậm độ hình tròn ở trung tâm (các đầu mũi tên). Hình CT sau tiêm thuốc tương phản (B) cho thấy bắt thuốc ngoại vi mỏng và trơn láng (mũi tên) của tổn thương hình tròn.
Hình 3. Áp xe não: Xung T1W axial (A) cho thấy một tổn thương tín hiệu thấp ở tiểu não (mũi tên) với tín hiệu cao dạng đường ở ngoại vi (các đầu mũi tên). Viền tín hiệu cao của khối tổn thương (mũi tên) là có tín hiệu thấp trên xung T2W (các đầu mũi tên) (B). Xung T1W sau tiêm thuốc tương phản (C) cho thấy bắt thuốc của viền tổn thương (mũi tên) và dọc theo não thất tư (đầu mũi tên), cho thấy tổn thương lan rộng vào trong não thất. Tổn thương (*) có tín hiệu rất sáng trên xung DWI (D) với tín hiệu cao tương tự dịch bên trong não thất (đầu mũi tên).
5. Bệnh não do ấu trùng Toxoplasma (Cerebral Toxoplasmosis)
*Dấu hiệu hình ảnh đặc hiệu
Ở những bệnh nhân bị suy giảm miễn dịch (immunocompromised), các tổn thương ở não do ấu trùng Toxoplasma sẽ biểu hiện trên CT không tiêm thuốc dưới dạng nhiều vùng giảm đậm độ, thường thấy nhất ở chất xám sâu (deep gray matter) và tại chỗ giáp ranh vỏ – tủy (corticomedullary junction). Các tổn thương bắt thuốc dạng nốt (nodular enhancement) hoặc dạng vòng (ring enhancement) trên hình CT và xung T1 sau tiêm thuốc tương phản. Các tổn thương bắt thuốc dạng vòng ở khoảng 1/3 số trường hợp cho thấy có một nốt lệch tâm bên trong (internal eccentric nodule), được gọi là “dấu hiệu bia bắn lệch tâm – eccentric target sign”, được coi là có độ đặc hiệu cao cho bệnh toxoplasmosis.
Các phần bắt thuốc của tổn thương thường đồng tín hiệu đến tín hiệu thấp trên T2W kèm phù mạch có tín hiệu cao xung quanh. Xuất huyết (Hemorrhage) đôi khi xuất hiện. Tổn thương hình cánh bướm (Butterfly lesions) xuyên qua thể chai (corpus callosum) cũng đã được mô tả. Tổn thương do bệnh toxoplasmosis cho thấy tín hiệu cao ở trung tâm trên bản đồ ADC, phù hợp với tăng sự khuếch tán, và thể tích máu não vùng tương đối (rCBV) là giảm trên hình ảnh tưới máu. MRI phổ (MRS) có xu hướng cho thấy đỉnh choline giảm ở mức độ vừa phải.
*Thông tin lâm sàng liên quan
Bệnh não do ấu trùng Toxoplasma (Cerebral toxoplasmosis) là nhiễm trùng cơ hội ở hệ thần kinh trung ương (CNS) thường gặp nhất ở bệnh nhân AIDS, những bệnh nhân dễ mắc bệnh nhất khi số lượng tế bào CD4 của họ giảm xuống dưới 100 tế bào/ml. Triệu chứng biểu hiện phổ biến nhất là đau đầu, thường đi kèm với sốt và thay đổi trạng thái tinh thần. Co giật, khiếm khuyết thị giác (visual field defects), bệnh lý thần kinh sọ não (cranial neuropathies), và các khiếm khuyết thần kinh khu trú khác cũng có thể xuất hiện.
Chẩn đoán thường dựa vào việc phát hiện trực tiếp vi sinh vật (thường thông qua khuếch đại PCR (PCR amplification)) trong dịch não tủy (CSF), máu, hoặc nước tiểu. Thallium-201 SPECT và FDG-PET có thể giúp phân biệt đáng tin cậy giữa lymphoma hệ thần kinh trung ương (CNS) với bệnh do ấu trùng Toxoplasma (toxoplasmosis) ở các tổn thương có kích thước > 2 cm, vì bệnh do ấu trùng Toxoplasma không hấp thụ chất phóng xạ. Các phác đồ điều trị (treatment regimens) hiện tại không thể tiêu diệt hoàn toàn vi sinh vật; do đó, bệnh nhân AIDS bị nhiễm ấu trùng Toxoplasma cần điều trị duy trì suốt đời để ngăn ngừa tái phát nhiễm trùng hoạt động.
*Chẩn đoán phân biệt
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Tín hiệu tối trên bản đồ ADC
+ rCBV tăng cao trên hình ảnh tưới máu
+ Choline tăng cao trên MRI phổ (MRS)
+ Sáng lên (hot) trên Thallium-201 SPECT và FDG-PET
– Khối u di căn não (Metastatic Neoplasms)
+ rCBV tăng cao trên hình ảnh tưới máu.
+ Choline tăng cao trên MRI phổ (MRS).
– Áp xe não do vi khuẩn sinh mủ (Pyogenic Abscess)
+ Phần lõi có tín hiệu rất sáng trên xung DWI.
*Kết luận
Bệnh do ấu trùng Toxoplasma (Toxoplasmosis) là bệnh nhiễm ký sinh trùng (parasitic infection) do động vật nguyên sinh nội bào Toxoplasma gondii gây ra. Ký sinh trùng này lây truyền sang người chủ yếu qua việc ăn phải nang trứng (oocysts) có trong thịt chưa nấu chín hoặc rau bị nhiễm ký sinh trùng, hoặc qua tiếp xúc với phân mèo (cat feces). Ở những người có hệ miễn dịch bình thường, nhiễm T. gondii thường không gây triệu chứng hoặc chỉ gây ra các triệu chứng giống cúm nhẹ, tự khỏi. Sau đó, nhiễm ấu trùng thường bước vào giai đoạn tiềm ẩn không triệu chứng, đặc trưng bởi sự tồn tại của vi sinh vật dưới dạng nang mô (tissue cysts) (bradyzoites) trong nhu mô não và cơ.
Người ta ước tính rằng có tới 75% dân số có huyết thanh dương tính với T. gondii. Bệnh não do nhiễm ấu trùng Toxoplasma ở bệnh nhân suy giảm miễn dịch thường là kết quả của sự tái hoạt động của nhiễm trùng tiềm ẩn; trước đây xảy ra ở tới 1/2 số bệnh nhân AIDS, nhưng tỷ lệ mắc bệnh đã giảm kể từ khi có sự ra đời của các phác đồ điều trị HAART.
Bệnh nhiễm ấu trùng Toxoplasma (Toxoplasmosis) gây viêm não hoại tử (necrotizing encephalitis), được đặc trưng về mặt bệnh học với nhiều ổ hoại tử (foci of necrosis) và các nốt vi thần kinh đệm (microglia nodules), không có sự hình thành ổ áp xe. Nhiều Toxoplasma tachyzoite ở trong và ngoài tế bào (dạng nhân lên nhanh chóng của ký sinh trùng) và các nang được thấy ở bên trong và kế cận các ổ hoại tử và bên trong cả mô não không bị ảnh hưởng bởi quá trình viêm. Việc xác định thể hoạt động (tachyzoites) là dấu hiệu chẩn đoán đặc hiệu cho nhiễm trùng đang hoạt động (active infection).
Hình 1. Bệnh não do ấu trùng Toxoplasma: Xung T2W axial (A) cho thấy tín hiệu cao ở nhiều vùng (các mũi tên) với phù mạch rõ rệt (*) và hiệu ứng khối ở thùy trán trái. Cũng có tín hiệu thấp dạng vòng (các đầu mũi tên) bên trong vùng phù. Tổn thương này có bắt thuốc dạng vòng (ring enhancement) trên xung T1W sau tiêm thuốc tương phản (B). Ghi nhận một nốt nhỏ bắt thuốc nằm ở ngoại vi của tổn thương thùy trán trái (mũi tên), đây là một ví dụ của “dấu hiệu bia bắn lệch tâm – eccentric target sign”.
Hình 2. Bệnh não do ấu trùng Toxoplasma: Xung T1W sau tiêm thuốc tương phản mặt phẳng coronal cho thấy các tổn thương bắt thuốc dạng vòng với các nốt nằm lệch tâm (các mũi tên). Có phù mạch hai bên (các đầu mũi tên).
Hình 3. Bệnh não do ấu trùng Toxoplasma: Xung T1W sau tiêm thuốc tương phản có xóa mỡ (FS) mặt phẳng coronal (A) ở bệnh nhân AIDS cho thấy một tổn thương bắt thuốc ở ngoại vi tại tiểu não (mũi tên) với một nốt lệch tâm (đầu mũi tên). Bản đồ ADC mặt phẳng axial (B) cho thấy một vùng lớn có tín hiệu cao kèm hiệu ứng khối ở trung tâm nằm ở hạch nền bên phải (các mũi tên) phù hợp với phù mạch. Có một vòng tín hiệu thấp bên trong (các đầu mũi tên) kèm tăng độ khuếch tán ở trung tâm.
Hình 4. Bệnh não do ấu trùng Toxoplasma: Xung T1W sau tiêm thuốc tương phản mặt phẳng axial từ kỹ thuật chụp GRE thể tích 3D (volumetric GRE acquisition) (hình A) cho thấy một khối ở hạch nền trái (mũi tên) có bắt thuốc ở ngoại vi và nốt bên trong. Có phù mạch với tín hiệu thấp rõ rệt xung quanh và hiệu ứng khối đi kèm. Hình ảnh tưới máu DSC MR tương ứng (hình B) cho thấy thể tích máu não tương đối là thấp của tổn thương (các mũi tên).
6. Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
*Dấu hiệu hình ảnh đặc hiệu
Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL) thường biểu hiện dưới tổn thương dạng khối trong trục đồng nhất, có giới hạn rõ, tăng đậm độ trên CT không tiêm thuốc tương phản và tín hiệu thấp đến đồng tín hiệu trên T2 (chủ yếu do mật độ tế bào cao). Tổn thương điển hình cho thấy bắt thuốc mạnh đồng nhất và độ khuếch tán rất thấp với tín hiệu tối đặc trưng trên bản đồ ADC.
Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL) cũng có thể biểu hiện với dạng thâm nhiễm lan rộng chủ yếu quanh mạch máu và có giới hạn không rõ. Phù mạch và hiệu ứng khối đi kèm thường hiện diện. PCNSL chủ yếu nằm ở các cấu trúc não sâu, các vùng quanh não thất, thể chai và vách trong suốt (septum pellucidum) có xu hướng lan rộng dọc theo chất trắng dưới màng não thất (subependymal white matter). Tổn thương có thể là đa ổ (multiple) và có thể thấy sự lan rộng của màng mềm (leptomeningeal spread). Tuy nhiên, PCNSL cũng có thể biểu hiện với các tổn thương hoại tử và thậm chí là xuất huyết chủ yếu ở những bệnh nhân suy giảm miễn dịch, thường là bệnh nhân bị nhiễm HIV.
Sự bắt thuốc tương phản của lymphoma cũng có thể thay đổi và trong một số trường hợp rất hiếm gặp thì có thể hoàn toàn không có bắt thuốc tương phản và đặc điểm này hay gặp hơn ở bệnh nhân đã được điều trị bằng steroid. Phù mạch và hiệu ứng khối đôi khi cũng có thể là rất nhẹ.
Hình ảnh tưới máu (Perfusion imaging) cho thấy thể tích máu não tương đối (rCBV) tăng; tuy nhiên, thấp hơn so với u thần kinh đệm độ cao (high-grade gliomas) hoặc di căn (metastases). FDG PET và SPECT cho thấy hoạt động chuyển hóa cao của lymphoma nguyên phát hệ thần kinh trung ương (PCNSL). Các tổn thương dao động tự phát (spontaneously fluctuating lesions) là hiếm gặp với những thay đổi về hình dạng, kích thước và vị trí đã được báo cáo.
*Thông tin lâm sàng liên quan
Biểu hiện lâm sàng là không đặc hiệu, liên quan đến thâm nhiễm các cấu trúc não hoặc hiệu ứng khối, thường có các triệu chứng tương đối nhẹ so với kích thước của tổn thương. Tiên lượng nói chung là xấu (poor) và bệnh tiến triển nhanh, đặc biệt ở bệnh nhân nhiễm HIV. Do các đặc điểm thâm nhiễm của lymphoma, hình ảnh MRI có xu hướng đánh giá thấp hơn mức độ của bệnh. FDG PET toàn thân (Body FDG PET) có thể phát hiện vị trí ác tính toàn thân ở một số bệnh nhân.
Tổn thương đáp ứng nhanh chóng và tạm thời với điều trị bằng thuốc steroid. Sinh thiết định vị (Stereotactic biopsy) được thực hiện, sau đó là hóa trị liều cao bằng methotrexate hoặc các thuốc khác có khả năng đi qua hàng rào máu não, thường kết hợp với xạ trị toàn bộ não. Bệnh thường hay tái phát, và rất hiếm khi bệnh nhân sống sót được lâu dài.
*Chẩn đoán phân biệt
– U nguyên bào thần kinh đệm đa hình (Glioblastoma Multiforme – GBM)
+ Thường hoại tử và không đồng nhất với kiểu bắt thuốc không đều.
+ Thể tích máu não vùng tương đối (rCBV) có giá trị rất cao trên hình ảnh tưới máu.
+ Giá trị ADC của khối u đặc bắt thuốc không thấp như giá trị của lymphoma nguyên phát hệ thần kinh trung ương (PCNSL).
– Hủy myelin dạng tạo khối (Tumefactive Demyelination)
+ Kiểu bắt thuốc tương phản dạng vòng không hoàn toàn.
+ Thường không có hoặc phù rất nhẹ.
+ rCBV thấp trên hình ảnh tưới máu.
– Bệnh não do nhiễm ấu trùng Toxoplasma (Toxoplasmosis)
+ Không lan rộng dưới màng não thất.
+ rCBV thấp trên hình ảnh tưới máu.
+ Giá trị ADC cao.
+ Giảm chuyển hóa trên PET và SPECT.
– Khối u não do di căn (Metastatic Neoplasm)
+ rCBV rất cao trên hình ảnh tưới máu
– Áp xe não (Abscess)
+ Giá trị ADC thấp của dịch mủ trong lõi hoại tử không bắt thuốc.
+ rCBV thấp trên hình ảnh tưới máu.
+ Vỏ bao bắt thuốc dạng vòng trơn láng.
+ MRI phổ (MRS) cho thấy các đỉnh axit amin.
*Kết luận
Ban đầu bệnh được cho là có mối liên hệ đặc trưng với bệnh nhân suy giảm miễn dịch và có tỷ lệ mắc cao ở những người nhiễm HIV, nhưng lymphoma nguyên phát ở hệ thần kinh trung ương (PCNSL) hiện nay cũng được ghi nhận với tần suất ngày càng tăng ở những người có hệ miễn dịch bình thường, thường ở độ tuổi 50 đến 70 tuổi (sixth and seventh decades). Bệnh chiếm 4 – 5% trong tổng số các khối u não nguyên phát, phần lớn trong số đó là lymphoma không Hodgkin tế bào B lớn lan tỏa.
Tổn thương đơn độc hoặc đa ổ có bắt thuốc nằm ở quanh não thất hoặc vùng nông của não là đặc điểm của lymphoma hệ thần kinh trung ương trong nhu mô não (parenchymal CNS lymphoma), chiếm 1/3 số lymphoma hệ thần kinh trung ương thứ phát (secondary CNS lymphomas) và chiếm gần 100% số lymphoma hệ thần kinh trung ương nguyên phát (PCNSL). Trong một số trường hợp rất hiếm, tổn thương có thể không được phát hiện trên chẩn đoán hình ảnh. Giá trị ADC thấp và khả năng hấp thụ FDG cao cho thấy bệnh sẽ tiến triển nhanh hơn, và thời gian sống của bệnh nhân sẽ ngắn hơn, trong khi bệnh nhân có kết quả lâm sàng cải thiện có thể cho thấy giá trị ADC giảm sau khi dùng methotrexate.
Tỷ lệ đáp ứng cao và cải thiện thời gian sống còn với liệu pháp hóa trị đã dẫn đến các chiến lược điều trị trì hoãn hoặc loại bỏ xạ trị, nhằm giảm nguy cơ gây độc thần kinh; tuy nhiên, điều này lại đi kèm với tỷ lệ tái phát cao hơn.
Hình 1. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Hình ảnh CT không tiêm thuốc tương phản cho thấy một khối tăng đậm độ ở lồi thể chai (hyperdense splenium mass) (các mũi tên) kèm phù mạch (các đầu mũi tên).
Hình 2. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Xung T1W sau tiêm thuốc tương phản (A) cho thấy một tổn thương bắt thuốc đồng nhất (mũi tên) nằm ở sâu trong bán cầu não trái với hiệu ứng khối và phù mạch (đầu mũi tên). Hạn chế khuếch tán bên trong khối u (mũi tên) và tăng khuếch tán ở vùng phù nề (các đầu mũi tên) trên bản đồ ADC (B).
Hình 3. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Xung T2W axial cho thấy một tổn thương đồng nhất thâm nhiễm (các mũi tên) lan rộng từ gối thể chai (genu of the corpus callosum) với hình ảnh “cánh bướm – butterfly”. Khối u tăng tín hiệu nhẹ kèm phù rất nhẹ.
Hình 4. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Xung T1W xóa mỡ (FS) sau tiêm thuốc tương phản cho thấy các vùng bắt thuốc không đều (patchy) và giới hạn không rõ (các mũi tên) và hiệu ứng khối lên não thất bên phải (đầu mũi tên).
Hình 5. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Xung T1W sau tiêm thuốc tương phản mặt phẳng coronal (A) cho thấy một khối u bắt thuốc ở não thất ba (mũi tên) lan theo lớp dưới màng não thất (subependyma) của hai não thất bên (các đầu mũi tên). Bản đồ ADC mặt phẳng axial (B) cho thấy khối u có hạn chế khuếch tán (mũi tên).
Hình 6. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Xung FLAIR mặt phẳng axial (A) cho thấy tăng tín hiệu (các mũi tên) xung quanh não thất tư. Xung T1W sau tiêm thuốc tương phản (B) cho thấy sự bắt thuốc dưới màng não thất và màng mềm (các đầu mũi tên).
Hình 7. Lymphoma nguyên phát hệ thần kinh trung ương (PCNSL): Hình ảnh CT không tiêm thuốc tương phản (A) cho thấy một khối u tăng đậm độ quanh não thất (mũi tên) kèm phù (đầu mũi tên). Hình ảnh sau tiêm thuốc tương phản (B) cho thấy nhiều tổn thương bắt thuốc mạnh (các mũi tên).
7. Hủy myelin dạng tạo khối (Tumefactive Demyelination)
*Dấu hiệu hình ảnh đặc trưng
Các đặc điểm giống với tổn thương dạng tạo khối của bệnh đa xơ cứng (multiple sclerosis) và quá trình hủy myelin khác được gọi là tổn thương hủy myelin dạng tạo khối (TDLs – tumefactive demyelinating lesions). Tổn thương hủy myelin dạng tạo khối thường nằm trong chất trắng của não với kích thước từ 1 cm đến >10 cm. Chúng có thể là một ổ (unifocal); tuy nhiên, thường có thêm các tổn thương khác xuất hiện cùng lúc hoặc theo thời gian.
Tổn thương hủy myelin dạng tạo khối hầu hết có phù xung quanh, nhưng thường phù rất nhẹ, và hiệu ứng khối thường thậm chí còn rất ít hơn. Tổn thương có tín hiệu thấp ở trung tâm trên T1 và phần ngoại vi của tổn thương có thể có tín hiệu sáng hơn trên hình ảnh chuyển dịch từ hóa (MTI – magnetization transfer imaging). Hầu như tất cả tổn thương hủy myelin dạng tạo khối (TDLs) đều bắt thuốc tương phản, có thể cùng vị trí với viền tín hiệu thấp trên T2. Bắt thuốc dạng vòng không hoàn toàn (“vòng hở – open ring”) cùng với tín hiệu hỗn hợp trên T2 với đồng tín hiệu và tín hiệu cao của các thành phần bắt thuốc, không liên quan đến vỏ não, và không có hiệu ứng khối là những đặc điểm rất đặc hiệu cho tổn thương hủy myelin dạng tạo khối (TDL), nhưng không phải lúc nào cũng xuất hiện.
Các cấu trúc giống mạch máu, có thể là tĩnh mạch, chạy xuyên qua tổn thương là dấu hiệu điển hình nhưng hiếm khi được thấy. Các đặc điểm đặc trưng khác là viền ngoại vi có tín hiệu sáng trên phim DWI (tín hiệu tối trên bản đồ ADC) và thể tích máu não vùng tương đối (rCBV) thấp trên hình ảnh tưới máu. Giảm đậm độ (hypodensity) trên CT của các vùng bắt thuốc trên MRI (viền bắt thuốc trên MRI không thể thấy rõ trên hình CT không tiêm thuốc) cũng rất đặc hiệu. Sự tăng cao đáng kể của glutamate và glutamine (Glx, ở mức 2.1–2.5 ppm) thường hiện diện đặc trưng trên MRI phổ (MRS – MR spectroscopy) với thời gian lặp ngắn (short echo time) (TE khoảng 30 ms). Các dấu hiệu không đặc hiệu thường được quan sát thấy với thời gian lặp trung bình (intermediate echo times).
*Thông tin lâm sàng liên quan
Tổn thương hủy myelin dạng tạo khối (TDL) có thể ảnh hưởng đến mọi lứa tuổi, nhưng thường gặp nhất ở người trẻ tuổi, thường là biểu hiện ban đầu của bệnh đa xơ cứng (MS). Biểu hiện thường có nhiều triệu chứng bao gồm mất ngôn ngữ (aphasia), mất nhận thức (agnosia), co giật và rối loạn thị giác.
Tổn thương hủy myelin dạng tạo khối (TDL) có thể cho thấy đáp ứng chậm hoặc không đáp ứng với steroid và tổn thương tiến triển trong vài tuần. Việc sử dụng các đặc điểm hình ảnh của tổn thương, chẩn đoán nên được đưa ra trong phần lớn các trường hợp, giúp tránh được việc sinh thiết não (brain biopsy), thủ thuật này không chỉ gây ra tác dụng phụ mà còn thường không giúp chẩn đoán.
*Chẩn đoán phân biệt
– U não nguyên phát (U thần kinh đệm độ cao) – Primary Brain Neoplasms (High-Grade Gliomas)
+ Các vùng bắt thuốc tương phản là không giảm đậm độ trên CT.
+ Phù thâm nhiễm (infiltrative edema) đến vỏ não và/hoặc chất xám sâu.
+ rCBV rất cao trên hình ảnh tưới máu.
+ Không có kiểu bắt thuốc dạng vòng không hoàn toàn.
+ Đỉnh Glx (glutamine và glutamate, “dạng gù vai – shoulder” của đỉnh NAA) không tăng trên MRI phổ (MRS).
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Tăng đậm độ trên hình CT không tiêm thuốc.
+ Thường bắt thuốc mạnh đồng nhất, không phải kiểu bắt thuốc dạng vòng không hoàn toàn.
+ Giá trị ADC rất thấp lan tỏa.
+ Thường tăng rCBV trên hình ảnh tưới máu.
+ Đỉnh Glx không tăng trên MRI phổ (MRS).
– Khối u não do di căn (Metastatic Neoplasm)
+ Bắt thuốc dạng vòng hoàn toàn hoặc dạng nốt.
+ Vị trí đặc trưng ở vùng vỏ não – dưới vỏ não.
+ rCBV tăng cao trên hình ảnh tưới máu.
+ Đỉnh Glx không tăng trên MRI phổ (MRS).
– Áp xe não
+ Phần lõi trung tâm có tín hiệu sáng trên xung DWI và tối trên bản đồ ADC.
+ Bắt thuốc dạng vòng hoàn toàn và bờ trơn láng.
+ Phù xung quanh thường nhiều.
*Kết luận
Dấu hiệu bệnh học phổ biến của tổn thương hủy myelin dạng tạo khối (TDL) bao gồm các tổn thương tăng sinh tế bào với tình trạng hủy myelin hợp lưu (confluent demyelination), nhiều đại thực bào bọt chứa các mảnh vụn myelin, tăng sinh tế bào hình sao phản ứng, bảo tồn sợi trục tương đối và tình trạng viêm tế bào lympho quanh mạch máu và trong nhu mô thay đổi. Các đại thực bào thâm nhiễm và tế bào hình sao phản ứng thường kết hợp chặt chẽ với nhau.
Các đặc điểm mô học có thể giống với khối u bao gồm tăng sinh tế bào, tế bào hình sao đa hình thái, nhân không điển hình, hình ảnh phân bào hiếm gặp và đôi khi có hoại tử hoặc thay đổi dạng nang. Chẩn đoán bệnh học có thể khó khăn, đặc biệt trên mẫu bệnh phẩm cắt lạnh (frozen-section specimen) ban đầu khi nghi ngờ chủ yếu là ác tính. Các đặc điểm mô học bổ sung hướng tới quá trình hủy myelin là không có hoại tử đông (coagulative necrosis), thay vào đó là các tế bào hình sao phản ứng tròn trịa được phân bố khá đều, một số có nhiều nhân nhỏ (tế bào Creutzfeldt) và không có tăng sinh vi mạch máu.
Hủy myelin dạng tạo khối cũng được mô tả ở bệnh nhân nhiễm HIV và là một dạng ít gặp của nhiễm độc thần kinh do tacrolimus.
Hình 1. Hủy myelin dạng tạo khối: Hình ảnh trên CT không tiêm thuốc tương phản (A) cho thấy một vùng hình bầu dục giảm đậm độ không có viền tăng đậm độ (mũi tên), vùng này bắt thuốc dạng vòng hở (mũi tên) trên CT có tiêm thuốc tương phản (B). Xung T2W (C) cho thấy tín hiệu rất cao của tổn thương và phù rất ít ở vùng kế cận (mũi tên). Viền ngoại vi của tổn thương rất sáng trên xung DWI (D). Phần lõi của tổn thương có tín hiệu thấp kèm viền ngoại vi bắt thuốc dạng vòng hở trên xung T1W sau tiêm thuốc tương phản (E).
Hình 2. Hủy myelin dạng tạo khối: Xung FLAIR mặt phẳng axial (A) cho thấy hai tổn thương chất trắng với phù dạng ngón tay (finger-like edema) ở ngoại vi (các mũi tên). Thể tích máu não vùng tương đối (rCBV) trong các tổn thương tương tự với chất trắng ở phía đối diện trên hình ảnh MRI tưới máu tương ứng (B). Có sự bắt thuốc dạng mảng và dạng nốt hình vòng cung (mũi tên) quanh não thất trên xung T1W mặt phẳng coronal sau tiêm thuốc tương phản (C).
Hình 3. Hủy myelin dạng tạo khối: Xung T2W mặt phẳng coronal (A) cho thấy bất thường chất trắng hai bên (các mũi tên) với cấu trúc bên trong không đồng nhất và có hiệu ứng khối nhẹ. Hình ảnh T1W sau tiêm thuốc tương phản (B) cho thấy các lớp bắt thuốc dạng mảng và vòng cung (các mũi tên). MRI phổ (MRS) với TE là 30 ms cho thấy đỉnh Glx nổi bật (mũi tên) nằm bên trái đỉnh NAA (đầu mũi tên).
Hình 4. Hủy myelin dạng tạo khối: Xung T1W dịch chuyển từ hóa (Magnetization transfer) (A) cho thấy một tổn thương hình tròn có tín hiệu thấp với viền ngoại vi có tín hiệu sáng hơn (mũi tên), viền nay bắt thuốc dạng vòng hở sau tiêm thuốc tương phản (B).
8. U lao (Tuberculoma)
*Dấu hiệu hình ảnh đặc hiệu
U lao (Tuberculomas) là tổn thương bắt thuốc dạng vòng (ring-enhancing lesions) có kích thước rất đa dạng, từ < 1cm đến vài cm. Mặc dù u lao thường được thấy ở bán cầu đại não nhưng chúng có thể xuất hiện ở bất cứ vị trí nào trong não, bao gồm cả tiểu não và thân não.
Trên CT, đậm độ của tổn thương thay đổi và được bao quanh bởi phù mạch với mức độ khác nhau. Có sự bắt thuốc tương phản của vỏ bao, trong khi vôi hóa được thấy ở khoảng 20% các u lao. Đôi khi, phần trung tâm của tổn thương chứa nốt bắt thuốc hoặc vôi hóa, tạo ra “dấu hiệu bia bắn – target sign”, rất gợi ý đến u lao.
Trên MRI, u lao với phần trung tâm hoại tử (necrotic center) cho thấy tín hiệu thấp trên T1 và tín hiệu cao trên T2, trong khi u lao có phần trung tâm đặc (solid center) có tín hiệu trung gian trên T1 và tín hiệu thấp trên T2 cùng với giá trị ADC thấp. Màng não dày lên và bắt thuốc nằm kế cận u lao giúp gợi ý chẩn đoán. Do đó, một tổn thương dạng áp xe (abscess-like lesion) có tín hiệu thấp ở trung tâm trên T2 gợi ý lao (tuberculosis) hoặc nấm (fungus). Trên hình ảnh xung T1W dịch chuyển từ hóa (magnetization transfer T1-weighted images) thì vỏ bao có tín hiệu cao.
Dấu hiệu trên MRI phổ (MRS) cho thấy nồng độ lipid và lactate tăng cao, NAA và creatine thấp với nồng độ choline thay đổi, nhưng không có axit amin nào (tăng axit amin gặp trong áp xe sinh mủ (pyogenic abscess)). Hình ảnh tưới máu cho thấy rCBV thấp. Nhồi máu não là thường gặp, đặc biệt là ở “vùng lao – tubercular zone” – nhân đuôi, đồi thị trước và chi trước bao trong.
*Thông tin lâm sàng liên quan
Hầu hết bệnh nhân bị u lao sẽ có viêm màng não do lao kèm theo (underlying tuberculous meningitis). Các dấu hiệu lâm sàng diễn ra âm thầm và không đặc hiệu với co giật tương đối thường gặp. Dịch não tủy (CSF) cho thấy protein cao, tăng số lượng bạch cầu (pleocytosis), glucose thấp và có thể khó tìm thấy vi sinh vật (microorganisms). Cấy dịch não tủy cho kết quả dương tính < 50% bệnh nhân và mất nhiều thời gian (4-8 tuần) để nuôi cấy vi sinh vật. Xét nghiệm da PPD (PPD skin test) thường âm tính, làm phức tạp chẩn đoán ban đầu. Xét nghiệm PCR đối với bệnh lao cho kết quả dương tính và rất hữu ích trong việc thiết lập chẩn đoán chính xác.
Hầu hết bệnh nhân còn trẻ và bệnh không phân biệt giới tính. Tỷ lệ mắc bệnh và di chứng là đáng kể, bao gồm co giật mạn tính, liệt, chậm phát triển tâm thần, não úng thủy và đột quỵ. Ngay cả khi được điều trị thích hợp, u lao cũng mất nhiều năm để thoái triển (resolve) và có thể cần phải phẫu thuật cắt bỏ. Bệnh lao ở thần kinh trung ương không được điều trị có thể gây tử vong và bệnh nhân có thể chết do nhiễm trùng nguyên phát hoặc do não úng thủy.
*Chẩn đoán phân biệt
– Áp xe do vi khuẩn sinh mủ (Pyogenic Abscess)
+ Tín hiệu cao ở trung tâm trên T2.
+ MRI phổ (MRS) cho thấy nhiều axit amin (như succinate và acetate).
– Khối u não (Nguyên phát hoặc thứ phát)
+ Vùng trung tâm hoại tử cho thấy độ khuếch tán cao mà không phải là hạn chế khuếch tán.
+ MRI phổ (MRS) cho thấy nồng độ choline cao.
– Nhiễm nấm (Fungal Infection); U hạt Sarcoidosis (Sarcoidosis Granuloma)
+ Có thể không phân biệt được.
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Thường bắt thuốc tương phản đồng nhất
+ rCBV tăng cao trên hình ảnh tưới máu
*Kết luận
Trên toàn thế giới, có hơn 10 triệu ca mắc bệnh lao được ghi nhận hằng năm và tỷ lệ mắc bệnh này ngày càng tăng do xu hướng di cư. Bệnh lao cũng phổ biến hơn ở những bệnh nhân bị suy giảm miễn dịch như bệnh nhân mắc bệnh AIDS. Khoảng 10% bệnh nhân lao có tổn thương hệ thần kinh trung ương (CNS). U lao là biểu hiện khu trú của nhiễm trùng lao (tuberculous infection) và có thể xảy ra trong hoặc ngoài trục.
U lao thường nằm trong trục (intra-axial) và xuất phát từ sự lây lan theo đường máu (hematogenous dissemination), thường là do nhiễm trùng phổi nguyên phát. U lao đứng thứ hai sau viêm màng não và là biểu hiện phổ biến nhất của bệnh lao hệ thần kinh trung ương. Vi sinh vật xâm nhập vào thành tĩnh mạch và động mạch, vào trong não thường ở vùng ranh giới chất xám và chất trắng. Kết quả là hình thành u hạt với vùng trung tâm hoại tử có bã đậu (caseating) hoặc không bã đậu hóa (non-caseating). Ban đầu có tình trạng viêm lan tỏa, nhưng cuối cùng hình thành vỏ bao dày chứa collagen.
Hình 1. U lao: Xung T2W mặt phẳng axial (A) ở bệnh nhân bị co giật cho thấy một tổn thương nhỏ hình bầu dục hơi giảm tín hiệu nằm ở vỏ não – vùng dưới vỏ não thùy thái dương trái (mũi tên) kèm tăng tín hiệu nhẹ xung quanh. Ngoài ra còn có một ổ nhồi máu lỗ khuyết mạn tính (chronic lacunar infarct) (đầu mũi tên) ở phần trước của đồi thị bên phải. Bản đồ ADC tương ứng (B) cho thấy tín hiệu tối của tổn thương (mũi tên), phù hợp với hạn chế khuếch tán, trong khi xung T1W sau tiêm thuốc tương phản (C) cho thấy bắt thuốc dạng viền (mũi tên). Có thêm sự bắt thuốc dọc theo rãnh sylvian (đầu mũi tên).
Hình 2. U lao: Xung T1W sau tiêm thuốc tương phản mặt phẳng axial (A) ở bệnh nhi cho thấy một tổn thương lớn nằm trong trục (mũi tên) có bắt thuốc dạng vòng không đều và phù xung quanh. Ngoài ra còn có sự bắt thuốc màng mềm (pial enhancement) (các đầu mũi tên) ở vùng này. Bản đồ ADC tương ứng (B) cho thấy tổn thương và một số mô kế cận có tín hiệu thấp do khuếch tán hạn chế. Ngoài ra còn có tín hiệu cao của vùng phù mạch xung quanh.
Hình 3. U lao: Xung T1W sau tiêm thuốc tương phản mặt phẳng axial (A) cho thấy một tổn thương bắt thuốc dạng vòng (mũi tên) ở bán cầu tiểu não phải. Một tổn thương bắt thuốc nhẹ ở bán cầu tiểu não trái (đầu mũi tên). Xung T2W (B) cho thấy các khối hai bên có tín hiệu thấp (các mũi tên) tương ứng với các tổn thương bắt thuốc.
Hình 4. U lao: Xung T1W sau tiêm thuốc tương phản mặt phẳng coronal cho thấy các tổn thương bắt thuốc dạng vòng (các mũi tên) và bắt thuốc màng mềm lan tỏa (diffuse leptomeningeal enhancement), thấy rõ nhất ở các bể nền sọ (các đầu mũi tên).
9. U thần kinh đệm ít nhánh (Oligodendroglioma)
*Dấu hiệu hình ảnh đặc hiệu
U thần kinh đệm ít nhánh (Oligodendrogliomas) thường là tổn thương trên lều có giới hạn rõ, xuất phát từ chất xám, thường gặp nhất là ở thùy trán. Các dấu hiệu điển hình trên CT bao gồm sự hiện diện của vôi hóa dạng đám (clumped) và dạng nốt (nodular) bên trong khối giảm đậm độ đến đồng đậm độ liên quan đến vỏ não. Thay đổi dạng nang thường xảy ra, trong khi xuất huyết trong u thì hiếm gặp.
U thần kinh đệm ít nhánh thường là tổn thương nằm ở vỏ não với tín hiệu thấp trên T1 và cao trên T2 kèm hiệu ứng khối nhẹ, và có thể thấy các vùng mất tín hiệu/ảnh giả nhạy từ trên xung T2* gây ra do vôi hóa. Sự xuất hiện các vùng mới có bắt thuốc tương phản và phù theo truyền thống trước đây được coi là dấu hiệu của chuyển dạng ác tính/không biệt hóa (anaplastic transformation) trong u thần kinh đệm; tuy nhiên, việc bắt thuốc tương phản cho thấy độ chính xác rất thấp trong việc phân biệt u thần kinh đệm ít nhánh không biệt hóa (anaplastic) với u thần kinh đệm ít nhánh độ thấp.
Ngoài ra, tăng thể tích máu não tương đối (rCBV) trên hình ảnh MRI tưới máu trên xung T2* sau tiêm thuốc tương phản (contrast-enhanced T2* MR perfusion) là một dấu hiệu của sự tiến triển nhanh và tiên lượng xấu ở bệnh nhân bị u thần kinh đệm, có thể thấy ở một số u thần kinh đệm ít nhánh độ thấp. Sự tăng kích thước của khối u trong vòng 6 tháng dường như là yếu tố tiên lượng hỗ trợ nhất cho sự tiến triển nhanh của khối u và tiên lượng xấu, là yếu tố tiên lượng chính xác hơn so với thể tích khối u ban đầu lớn hay rCBV cao. Tín hiệu không đồng nhất, bờ không đều và rCBV cao của khối u có tính gợi ý về đột biến mất đoạn 1p/19q, điều này có liên quan đến đáp ứng điều trị tốt hơn.
*Thông tin lâm sàng liên quan
Biểu hiện lâm sàng thường gặp nhất của u thần kinh đệm ít nhánh là co giật, thường kéo dài vài năm. Tỷ lệ mắc bệnh cao nhất là vào khoảng thập kỷ thứ 5 của cuộc đời (từ 40 đến dưới 50 tuổi) và tổn thương này thường gặp hơn ở nam giới một chút. Chụp MRI đa phương thức theo chiều dọc nối tiếp (Serial longitudinal multimodality MR imaging) bao gồm MRI thông thường (conventional MRI), MRI phổ (MR spectroscopy), MRI tưới máu và khuếch tán đã được sử dụng để phát hiện sự chuyển đổi từ khối u độ thấp (low grade) sang khối u độ cao (high grade).
*Chẩn đoán phân biệt
– U sao bào (Astrocytoma)
+ Ít khi có vôi hóa
+ Liên quan chủ yếu đến chất trắng
– U thần kinh đệm hạch (Ganglioglioma)
+ Vị trí thường gặp nhất ở thùy thái dương
+ Thành phần dạng nang rất thường gặp
– U thần kinh biểu mô loạn sản phôi (Dysembryoplastic Neuroepithelial Tumor – DNET)
+ Tổn thương nằm ở vỏ não có hình dạng “bọt bong bóng – bubbly”, có thể có hình chêm
+ Không có hiệu ứng khối và không bắt thuốc
– U sao bào vàng đa hình (Pleomorphic Xanthoastrocytoma – PXA)
+ Thường có thành phần dạng nang lớn với phần mô đặc áp sát bề mặt màng mềm.
+ Dấu hiệu “đuôi màng cứng – dural tail” thường hiện diện.
+ Có thể gây ăn mòn (scalloping) vào mặt trong của xương sọ kế cận.
– Viêm não (Cerebritis)
+ Tăng tín hiệu ở vỏ não/vùng dưới vỏ não trên T2 và bắt thuốc dạng hồi não.
+ Có hạn chế khuếch tán trên bản đồ ADC.
– Nhồi máu não giai đoạn cấp đến bán cấp (Acute to Subacute Infarct)
+ Thường có bất thường tín hiệu dạng hình chêm ở vỏ não/vùng dưới vỏ não.
+ Theo vùng phân bố mạch máu.
+ Có hạn chế khuếch tán trong giai đoạn cấp.
+ Nếu có bắt thuốc thì bắt thuốc thường theo dạng hồi não.
*Kết luận
U thần kinh đệm ít nhánh bao gồm cả u thần kinh đệm ít nhánh đơn thuần (pure oligodendroglioma) và u hỗn hợp thần kinh đệm ít nhánh và tế bào hình sao (mixed oligoastrocytoma), là loại u thần kinh đệm phổ biến thứ hai ở người lớn sau u nguyên bào thần kinh đệm (glioblastoma). U thần kinh đệm ít nhánh đơn thuần (pure oligodendroglioma) có kết quả điều trị tốt hơn và thời gian sống còn lâu hơn so với u sao bào (astrocytomas) và u hỗn hợp thần kinh đệm ít nhánh và tế bào hình sao (mixed oligoastrocytoma). Thời gian sống còn trung bình ước tính khoảng 10 năm đối với u thần kinh đệm ít nhánh độ thấp và 4 năm đối với u thần kinh đệm ít nhánh không biệt hóa/độ cao. Tình trạng mất tính dị hợp tử (heterozygosity)/mất đoạn (deletions) ở nhiễm sắc thể 1p và 19q được thấy ở một số khối u có liên quan đến cả đáp ứng điều trị được cải thiện và thời gian sống lâu hơn.
U thần kinh đệm ít nhánh xuất phát từ sự biến đổi tân sinh (neoplastic transformation) của tế bào thần kinh đệm ít nhánh hoặc tế bào tiền thân thần kinh đệm chưa trưởng thành. Diễn tiến tự nhiên của u thần kinh đệm ít nhánh độ thấp là tiến triển thành u thần kinh đệm độ cao với khoảng thời gian thay đổi giữa chẩn đoán và sự chuyển dạng không biệt hóa (ác tính). U thần kinh đệm ít nhánh không biệt hóa (Anaplastic oligodendrogliomas) cũng thường được chẩn đoán ngay từ đầu (de novo).
U thần kinh đệm ít nhánh độ thấp có đặc điểm mô học là sự hiện diện của mạng lưới các mao mạch phân nhánh bên trong mô đệm của chúng, được mô tả có hình dạng giống như “dạng lưới hình mắt cáo – chicken wire”, điều này giải thích cho dấu hiệu điển hình là tăng rCBV ở những khối u tân sinh này. Chuyển dạng không biệt hóa (Anaplastic transformation) của khối u được đặc trưng bởi sự gia tăng tế bào, không điển hình rõ rệt và hoạt động phân bào cao, tăng sản nội mô và tăng sinh vi mạch trong u. Các khối u này hiếm khi di căn ra ngoài hệ thần kinh trung ương.
Hình 1. U thần kinh đệm ít nhánh (Oligodendrogliomas): Hình ảnh trên CT axial (A) cho thấy một vùng giảm đậm độ kín đáo ở vỏ não – vùng dưới vỏ não thùy trán trái (các mũi tên) với một vài vùng có vôi hóa thô (coarse calcifications) (các đầu mũi tên). Hình ảnh MRI xung FLAIR axial ở lát cắt nằm ở mức cao hơn một chút (B) cho thấy một vùng tăng tín hiệu có giới hạn rõ chủ yếu liên quan đến cả chất xám và chất trắng với hiệu ứng khối nhẹ biểu hiện qua sự hẹp lại tương đối của các rãnh vỏ não. Các dấu hiệu này phù hợp với phù thâm nhiễm. Ghi nhận tổn thương chủ yếu liên quan đến vỏ não. Bản đồ ADC (C) tương ứng với lát cắt ngang mức ở hình A cho thấy sự khuếch tán tăng tương đối trong khối u (các mũi tên) có tín hiệu cao hơn so với nhu mô não bình thường. Bản đồ thể tích máu não vùng tương đối (rCBV) (D) ở lát cắt ngang mức này trên MRI tưới máu xung T2* sau tiêm thuốc tương phản cho thấy sự tăng tương đối thể tích máu não bên trong tổn thương (các mũi tên).
Hình 2. U thần kinh đệm ít nhánh (Oligodendrogliomas): Xung FLAIR axial (A) cho thấy một tổn thương tăng tín hiệu ở vỏ não – vùng dưới vỏ não (các mũi tên) chủ yếu liên quan đến thùy đảo (insula) và thùy thái dương (temporal lobe) trái với hiệu ứng khối nhẹ và một vùng dạng nang bên trong (các đầu mũi tên). Xung T1W sau tiêm thuốc tương phản tương ứng (B) cho thấy các vùng bắt thuốc vỏ não dạng đường kín đáo (các đầu mũi tên) bên trong tổn thương.
Hình 3. U tế bào thần kinh đệm ít nhánh (Oligodendrogliomas): Xung FLAIR cho thấy một khối u nằm trong não thất liên quan đến đồi thị hai bên (các mũi tên). Nhiều vùng có tín hiệu rất thấp (các đầu mũi tên) biểu thị cho mạch máu và vôi hóa.
10. U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma)
*Dấu hiệu hình ảnh đặc hiệu
MRI là phương thức chẩn đoán hình ảnh được lựa chọn cho u sao bào lan tỏa độ thấp và mức độ của tổn thương được xác định tốt nhất trên xung FLAIR. U sao bào lan tỏa độ thấp thường là khối u nằm trong trục (intra-axial masses) đồng nhất với trung tâm của khối u (epicenter) nằm trong chất trắng và hiệu ứng khối từ rất nhẹ đến nhẹ. Khối u có thể được thấy ở tất cả các phần của não trên lều, thường gặp ở thùy đảo. Khối u thường có giới hạn rõ với tín hiệu cao trên T2 và tín hiệu thấp hoặc đồng tín hiệu trên T1, thâm nhiễm và lan rộng đến não bên dưới; tuy nhiên, giới hạn của u trong một số trường hợp có thể kém rõ.
U sao bào lan tỏa độ thấp thường có tín hiệu sáng trên bản đồ ADC, phù hợp với tăng độ khuếch tán, và thường không bắt thuốc tương phản. Trên hình ảnh tưới máu, khối u cho thấy thể tích máu não tương đối (rCBV) thấp, trung bình chỉ cao hơn một chút so với não bình thường. MRI phổ (MRS) thường cho thấy nồng độ NAA giảm với choline tăng nhẹ và không có lactate. U sao bào lan tỏa độ thấp thường hơi giảm đậm độ hơn so với não bình thường trên hình CT.
*Thông tin lâm sàng liên quan
Bệnh nhân thường là người trẻ tuổi bị co giật mà không có triệu chứng nào khác, hoặc thậm chí không có triệu chứng với tổn thương được phát hiện tình cờ trên xét nghiệm hình ảnh. Khối u này trải qua quá trình chuyển dạng ác tính (malignant transformation) được biểu hiện bằng sự suy giảm trên lâm sàng (clinical decline) và tiến triển trên chẩn đoán hình ảnh. Không có sự đồng thuận về cách điều trị tốt nhất cho người lớn bị u thần kinh đệm độ thấp; điều trị thường bao gồm phẫu thuật cắt bỏ, có thể theo sau là hóa trị. Ngoài ra, khối u có thể được theo dõi bằng hình ảnh sau khi sinh thiết ban đầu, vì bệnh nhân có thể trì hoãn phẫu thuật cho đến khi có sự tiến triển hoặc thay đổi về chất lượng cuộc sống.
*Chẩn đoán phân biệt
– Loạn sản vỏ não khu trú (Focal Cortical Dysplasia)
+ Có sự dày lên của chất xám.
+ Kèm theo tăng tín hiệu đồng nhất vùng dưới vỏ não có thể thuôn dài (taper) về phía não thất.
+ Không có hiệu ứng khối.
+ Vị trí thường gặp hơn ở thùy trán.
– U thần kinh đệm ít nhánh (Oligodendroglioma)
+ Nằm ở ngoại vi với thâm nhiễm lan rộng vào vỏ não ở thùy trán hoặc thùy thái dương.
+ Thường có vôi hóa
+ Có thể có rCBV (thể tích máu não tương đối) tăng trên hình ảnh tưới máu.
+ Có thể không phân biệt được giữa u sao bào lan tỏa độ thấp với u thần kinh đệm ít nhánh.
– U sao bào lông (Pilocytic Astrocytoma)
+ Hầu như luôn nằm ở hố sau (posterior fossa) hoặc vùng dưới đồi (hypothalamic region).
+ Thường bắt thuốc mạnh, ít nhất là một phần bắt thuốc.
+ Có thể biểu hiện dưới dạng nang với nốt ở thành bắt thuốc.
+ Thường được thấy ở trẻ em.
– U nguyên bào thần kinh đệm đa hình (Glioblastoma Multiforme)
+ Thường là khối u rất không đồng nhất.
+ Hầu như luôn bắt thuốc mạnh và không đồng nhất.
+ Các phần hoại tử rất thường gặp.
+ Hiệu ứng khối và phù nổi bật.
*Kết luận
U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma) là khối u não nguyên phát, phát triển chậm và có tính thâm nhiễm. Theo phân loại WHO năm 2007, u sao bào lan tỏa độ thấp bao gồm các biến thể dạng sợi (fibrillary), dạng tế bào phình to (gemistocytic), và dạng nguyên sinh chất. U sao bào lan tỏa độ thấp được xếp là độ II, khác với u thần kinh đệm khu trú độ I như u sao bào lông và u sao bào vàng đa hình. Phân độ của u sao bào (astrocytic tumors) dựa trên sự dị hình của tế bào học (cytological atypia) được xếp là độ II, trong khi khối u có tính không biệt hóa (anaplasia) và hoạt động phân bào được xếp là độ III. Khối u độ II theo WHO cũng bao gồm u thần kinh đệm ít nhánh và u thần kinh đệm ít nhánh – tế bào sao hỗn hợp.
Các khối u này chuyển dạng sang độ cao hơn (higher grade) theo thời gian, với thời gian sống còn trung bình là 5 – 10 năm. Đột biến gen p53 (p53 mutations) là biến đổi đầu tiên có thể phát hiện được ở phần lớn các u sao bào (astrocytomas) sẽ tiếp tục biến đổi. Các phép đo thể tích máu não tương đối (rCBV) trên hình ảnh MRI tưới máu tương quan tốt với thời gian tiến triển hoặc tử vong và giá trị rCBV cao dường như dự đoán sự tiến triển nhanh chóng ở u sao bào lan tỏa độ thấp. Hình ảnh MRI thông thường (Conventional MRI) đánh giá không đầy đủ (underestimates) mức độ của u lan rộng và việc cắt bỏ “siêu toàn bộ – supratotal” mở rộng với đường bờ cắt vượt ra ngoài tổn thương mà tổn thương này đã được xác định trên MRI có thể cải thiện kết quả.
Hình 1. U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma): Xung FLAIR mặt phẳng axial (A) cho thấy một tổn thương tăng tín hiệu nằm ở sâu (mũi tên) tập trung ở thùy đảo trái với hiệu ứng khối nhẹ, đẩy lệch cầu nhạt (globus pallidus) (*), và phần vỏ não phía trên hầu như được bảo tồn (đầu mũi tên). Tổn thương (mũi tên) có giới hạn tương đối rõ và giảm tín hiệu trên xung T1W sau tiêm thuốc tương phản tương ứng (B) có bắt thuốc tương phản rất nhẹ (đầu mũi tên). Bản đồ MRI tưới máu rCBV (C) cho thấy các giá trị tương tự ở tổn thương (các mũi tên) và não đối bên bình thường.
Hình 2. U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma): Xung FLAIR (A) ở bệnh nhân 34 tuổi bị co giật cho thấy một tổn thương tăng tín hiệu có giới hạn rõ (mũi tên) với hiệu ứng khối nhẹ, xuất phát từ chất trắng thùy trán phải. Vỏ não phía trên có vẻ được bảo tồn (đầu mũi tên). Tổn thương có tín hiệu sáng đồng nhất trên bản đồ ADC tương ứng (B). Tín hiệu thấp hơn của vỏ não tương đối còn nguyên vẹn (các đầu mũi tên). Không có sự bắt thuốc (C) trên xung T1W sau tiêm thuốc tương phản.
Hình 3. U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma): Xung FLAIR (A) cho thấy một tổn thương thâm nhiễm tăng tín hiệu (mũi tên) có giới hạn không rõ. Tổn thương cho thấy sự khuếch tán cao trên bản đồ ADC (B) và giảm tín hiệu với không bắt thuốc trên xung T1W sau tiêm thuốc tương phản (C).
11. Bệnh lý u thần kinh đệm lan tỏa (Gliomatosis Cerebri)
*Dấu hiệu hình ảnh đặc hiệu
Bệnh lý u thần kinh đệm lan tỏa (Gliomatosis Cerebri – GC) có đặc điểm chính là sự thâm nhiễm lan tỏa, liên quan đến >/= 3 thùy não liền kề nhau mà vẫn bảo tồn cấu trúc não. Khối u có đậm độ thấp trên CT và có thể làm chất trắng dày lên, đặc biệt là thể chai. Bắt thuốc trên CT và xuất huyết là hiếm gặp. Hình ảnh CT đôi khi có thể bình thường, và MRI là phương pháp chẩn đoán hình ảnh được lựa chọn.
Khối u có tín hiệu thấp trên T1 và tín hiệu cao trên T2. Vỏ não bị ảnh hưởng đặc trưng và thân não cũng có thể bị ảnh hưởng. Bắt thuốc tương phản là hiếm gặp và có thể phân bố không đồng đều. Kiểu MRI phổ (MRS) thay đổi tùy theo vùng, cho thấy mức choline bình thường hoặc thậm chí thấp, n-acetyl aspartate (NAA) thấp, cùng với myo-inositol cao và có thể cả creatine. Các vùng khác có thể cho thấy mức choline tăng.
Hình ảnh tưới máu cho thấy thể tích máu não tương đối (rCBV) bình thường hoặc giảm nhẹ. Sự khuếch tán (Diffusion) bên trong tổn thương thường tăng, và hình ảnh DTI có thể cho thấy bảo tồn hướng khuếch tán (directionality) nhưng độ bất đẳng hướng phân đoạn (fractional anisotropy) giảm. Sự lan rộng dưới màng mềm của bệnh lý u thần kinh đệm lan tỏa (GC) là rất hiếm.
*Thông tin lâm sàng liên quan
Đây là khối u hay gặp ở người trưởng thành (adults) với hầu hết các trường hợp thấy ở độ tuổi 40 đến 50, nhưng nó cũng có thể xảy ra ở bất kỳ lứa tuổi nào. Các triệu chứng biểu hiện không đặc hiệu và bao gồm các triệu chứng của tổn thương bó dài (long tract symptoms), sa sút trí tuệ, đau đầu (thường do não úng thủy gây ra) và co giật (cho thấy thâm nhiễm của vỏ não).
Tổn thương thân não có thể dẫn đến nhiều khiếm khuyết dây thần kinh sọ và thâm nhiễm thể chai có thể gây ra các thay đổi trong tính cách. Đây là một bệnh lý hiếm gặp với tỷ lệ mắc bệnh chính xác chưa được biết, và chẩn đoán ban đầu thường bị bỏ sót. Chẩn đoán xác định trước đây thường được thực hiện qua khám nghiệm tử thi, trong khi hiện nay sinh thiết cho thấy u sao bào (astrocytoma) cùng với chẩn đoán hình ảnh có thâm nhiễm từ 3 thùy não trở lên đã đủ để chẩn đoán.
Bệnh lý u thần kinh đệm lan tỏa (GC) là một quá trình tiến triển, dẫn đến tử vong ở > 50% bệnh nhân trong vòng 1 năm. Các phác đồ hóa trị (chemotherapy) và hóa xạ trị (chemoradiotherapy) gần đây cho thấy có hiệu quả ở bệnh nhân bị bệnh lý u thần kinh đệm lan tỏa (GC). Không có thâm nhiễm đối xứng hai bên và các đột biến gen nhất định (IDH1) có liên quan đến thời gian sống còn kéo dài.
*Chẩn đoán phân biệt
– Viêm não do Herpes (Herpes Encephalitis)
+ Các vùng bị tổn thương cho thấy hạn chế khuếch tán: tín hiệu sáng trên DWI và tối trên bản đồ ADC.
+ Tổn thương thường ở cả hai bên nhưng riêng biệt, không lan ra liên tục.
+ Bắt thuốc và xuất huyết có thể xuất hiện.
+ Biểu hiện lâm sàng thường là cấp đến bán cấp, có thể có sốt.
– Viêm não hệ viền (Limbic Encephalitis)
+ Hiệu ứng khối rất nhẹ hoặc không có.
+ Thường ở cả hai bên nhưng không lan ra liên tục.
+ Bắt thuốc và hạn chế khuếch tán có thể xuất hiện.
+ Có thể đã biết bệnh lý ác tính toàn thân.
– U sao bào lan tỏa độ thấp (Low-Grade Diffuse Astrocytoma)
+ Không lan rộng vào 3 thùy não
+ Không thể phân biệt được về mặt mô học
– Lymphoma nguyên phát hệ thần kinh trung ương (Primary CNS Lymphoma)
+ Bắt thuốc tương phản mạnh.
+ Đặc trưng là tăng đậm độ trên CT và có tín hiệu tối trên bản đồ ADC.
– Viêm não Rasmussen (Rasmussen Encephalitis)
+ Teo não tiến triển có thể xuất hiện sau giai đoạn phù ban đầu.
+ Đặc trưng là ở một bên.
+ Thường gặp ở trẻ em.
*Kết luận
Bệnh lý u thần kinh đệm lan tỏa (GC) là bệnh lý có nguồn gốc từ tế bào thần kinh đệm, được WHO coi là một phần của dòng u sao bào. Bệnh ảnh hưởng đến 3 thùy não trở lên và tiêu chuẩn hình ảnh rất quan trọng cho việc chẩn đoán chính xác vì mô học không đặc hiệu, thường cho thấy u sao bào thâm nhiễm (infiltrative astrocytoma) (WHO grade II). Có sự thâm nhiễm của u lan rộng với cấu trúc giải phẫu bên dưới được bảo tồn, dẫn đến sự phì đại (enlargement) của các phần não bị ảnh hưởng.
Không có hoại tử hoặc tân sinh mạch máu (neovascularity) khi chẩn đoán ở dạng cổ điển (classical form) (type I) là khối u grade III theo WHO, được phản ánh qua việc không có bắt thuốc tương phản và giảm tưới máu. Bắt thuốc khu trú và tăng rCBV được quan sát thấy ở dạng khối u khu trú của GC type II. Bệnh lý u thần kinh đệm màng mềm (Leptomeningeal gliomatosis) thậm chí còn ít gặp hơn và biểu hiện với bắt thuốc màng mềm lan tỏa của não và tủy sống, sau đó là sự phát triển các tổn thương trong nhu mô với sự thâm nhiễm lan rộng.
Hình 1. Bệnh lý u thần kinh đệm lan tỏa (GC): Xung T1W sau tiêm thuốc tương phản mặt phẳng axial (A) cho thấy một tổn thương tín hiệu thấp không bắt thuốc với hiệu ứng khối nhẹ, thâm nhiễm vào thùy thái dương, thùy đảo và hạch nền bên phải cũng như cả hai thùy trán (các mũi tên). Ngoài ra còn thấy tổn thương đồi thị trái (các đầu mũi tên). Xung FLAIR mặt phẳng axial (B) ở ngang mức tương ứng cho thấy tổn thương có tín hiệu cao và lan vào gối thể chai (*) đi ngang qua đường giữa. Ghi nhận tổn thương lan đến vỏ não thùy đảo (mũi tên). Xung FLAIR ở ngang mức cao hơn (C) cho thấy bất thường ở phần trước thể chai, cả hai thùy trán và thùy đảo bên phải. Xung FLAIR ở ngang mức thấp hơn (D) cho thấy tổn thương thùy thái dương trong và trước bên phải (các mũi tên). Sự thâm nhiễm tăng tín hiệu của chất xám vỏ não có thể thấy rõ.
Hình 2. Bệnh lý u thần kinh đệm lan tỏa (GC): Xung FLAIR mặt phẳng axial (A) cho thấy tăng tín hiệu kèm hiệu ứng khối ảnh hưởng đến chất trắng và chất xám của thùy chẩm và thùy thái dương sau bên trái (các mũi tên), và cả vùng xung quanh mép trước (anterior commissure) bên trái (đầu mũi tên). Bản đồ thể tích máu não tương ứng (B) trên hình ảnh MRI tưới máu T2* động học (dynamic) sau tiêm thuốc tương phản cho thấy rCBV thấp trên toàn bộ tổn thương (các mũi tên).
12. U sao bào vàng đa hình (Pleomorphic Xanthoastrocytoma – PXA)
*Dấu hiệu hình ảnh đặc hiệu
U sao bào vàng đa hình (Pleomorphic xanthoastrocytomas – PXAs) thường biểu hiện dưới dạng khối u dạng nang (cystic masses) nằm ở phía ngoại vi của bán cầu não trên lều (60%) với phần đặc tiếp giáp với màng não. Nốt đặc (solid nodule) bắt thuốc tương phản và có thể tạo ra hiện tượng bắt thuốc dạng “đuôi màng cứng – dural tail” (70%) hoặc khuyết lõm (scalloping) vào bản sọ trong của xương sọ kế cận.
U sao bào vàng đa hình hay gặp nhất ở thùy thái dương, thùy trán, và thùy đỉnh, nhưng có thể xuất hiện ở bất kỳ vị trí nào trong bán cầu não, và thậm chí trong não thất. Kích thước và mức độ bắt thuốc tương phản của PXA thay đổi, và hiếm khi có vôi hóa và xuất huyết. Trên MRI, tín hiệu của khối u đặc có thể thay đổi nhưng thành phần nang hầu như luôn có tín hiệu tương đương dịch não tủy (CSF) trên tất cả các chuỗi xung. Hiếm khi có xâm lấn não, di căn, và/ hoặc hoại tử.
*Thông tin lâm sàng liên quan
U sao bào vàng đa hình (PXA) là khối u ở người trẻ tuổi (với khoảng 60% được phát hiện < 18 tuổi) không phân biệt giới tính. Đây là khối u phát triển chậm, thường biểu hiện với các cơn co giật mạn tính, đau đầu và chóng mặt. Tỷ lệ sống còn là > 70% sau 10 năm kể từ khi chẩn đoán ban đầu, tuy nhiên PXA có thể thoái hóa thành độ ác tính cao hơn.
Phẫu thuật là phương pháp điều trị được lựa chọn, với việc cắt bỏ toàn bộ đại thể khối u (gross total resection) mang lại kết quả tốt nhất, và cắt bỏ lại (re-resection) được thực hiện cho các trường hợp tái phát. Hóa trị và xạ trị có thể được sử dụng cho khối u không thể cắt bỏ được (unresectable tumors) cũng như cho PXA không biệt hóa (anaplastic PXAs) nguyên phát và tái phát, nhưng vai trò của chúng chưa được xác định rõ ràng. Các đặc điểm duy nhất tương quan với thời gian sống còn là mức độ cắt bỏ khối u ban đầu và tốc độ phân bào.
*Chẩn đoán phân biệt
– U thần kinh đệm hạch (Ganglioglioma)
+ Vôi hóa ở 50% trường hợp.
+ Không có dấu hiệu “đuôi màng cứng – dural tail”.
+ Bắt thuốc thường ít hơn.
+ Có thể không phân biệt được (khối u có các thành phần của cả hai đã được mô tả)
– U thần kinh biểu mô loạn sản phôi (Dysembryoplastic Neuroepithelial Tumor – DNET)
+ Hình dạng đa nang “bọt xà phòng – bubbly”.
+ Không có nốt đặc bắt thuốc rõ.
+ Hiệu ứng khối rất nhẹ hoặc không có.
+ Bắt thuốc tương phản là rất hiếm.
– U sao bào lông (Pilocytic Astrocytoma)
+ Thường gặp hơn ở tiểu não hoặc vùng dưới đồi (hypothalamic)/vùng trên yên (suprasellar).
+ Không có dấu hiệu “đuôi màng cứng”.
+ Tín hiệu rất sáng trên bản đồ ADC.
– U thần kinh đệm ít nhánh (Oligodendroglioma)
+ Chủ yếu là khối u ở vỏ não
+ Thường có vôi hóa
– U thần kinh đệm hạch xơ hóa ở trẻ sơ sinh (Desmoplastic Infantile Ganglioglioma)
+ Tổn thương màng cứng nổi bật, kích thước rất lớn, nằm ngoài trục.
+ Nhiều tổn thương là thường gặp.
+ Ở trẻ nhỏ hơn.
*Kết luận
U sao bào vàng đa hình (PXA) chiếm < 1% trong số tất cả các khối u nguyên phát trong sọ (intracranial primary tumors). Về mặt mô học, chúng chứa nhiều tế bào khổng lồ đa hình (pleomorphic giant cells), tế bào hình thoi (spindle cells), và tế bào bọt (foamy cells) biểu hiện protein axit sợi thần kinh đệm (glial fibrillary acidic protein) và nằm trong một mạng lưới của các sợi lưới (reticulin) và thể hạt ưa eosin (eosinophilic granular bodies). U sao bào vàng đa hình (PXA) nằm ở vị trí nông ảnh hưởng đến màng não (meninges) và có thể bắt nguồn từ tế bào hình sao dưới màng mềm. Hiếm khi u sao bào vàng đa hình (PXA) xuất hiện ở tiểu não, tủy sống, và võng mạc (retina) nhưng hầu hết được thấy ở bán cầu đại não.
Không có nguyên nhân cụ thể hoặc đột biến di truyền (genetic aberrations) nào. U sao bào vàng đa hình (PXA) là khối u grade II theo WHO, được xem là “khu trú – localized” và do đó có thể cắt bỏ hoàn toàn được. Đôi khi u sao bào vàng đa hình (PXA) xâm lấn vào não và có thể được xếp là grade III. Quan trọng hơn, có tới 20% trong số chúng thoái hóa thành độ ác tính cao hơn. Hoạt động phân bào cao (5 lần phân bào trở lên trên 10 trường năng lượng cao) là đặc điểm chính của dạng không biệt hóa/grade cao.
Hình 1. U sao bào vàng đa hình (PXA): Xung T2W mặt phẳng axial cho thấy một khối u ở thùy thái dương trái có tín hiệu cao nhẹ (mũi tên) kèm một vùng có tín hiệu rất cao (đầu mũi tên), có thể là khối u dạng nang. Xung T1W mặt phẳng coronal sau tiêm thuốc tương phản (B) cho thấy sự bắt thuốc của phần đặc (đầu mũi tên) và thành của nang (mũi tên ngắn). Ngoài ra còn có dấu “đuôi màng cứng – dural tail” có bắt thuốc (mũi tên dài).
Hình 2. U sao bào vàng đa hình (PXA): Xung FLAIR mặt phẳng coronal (A) ở bệnh nhân trẻ tuổi bị co giật cho thấy một khối u không đồng nhất có tín hiệu cao nhẹ (mũi tên) ảnh hưởng đến cả chất xám và chất trắng ở thùy thái dương trong phải và lan rộng ra bề mặt não. Xung T1W sau tiêm thuốc tương phản ở ngang mức tương ứng (B) cho thấy tổn thương bắt thuốc mạnh (mũi tên), đặc biệt là ở phần ngoại vi của khối u.
Hình 3. U sao bào vàng đa hình (PXA): Một khối u kích thước lớn ở thùy trán – đỉnh phải (mũi tên) với các phần có thể là nang được thấy trên xung T2W mặt phẳng axial (A) ở ngang mức vành tia (corona radiata). Tổn thương được xác định rõ với phù mạch xung quanh ít (các đầu mũi tên). Xung T1W sau tiêm thuốc tương phản tương ứng (B) cho thấy sự bắt thuốc của phần đặc trong khối u dạng nang một phần này.
13. U thần kinh đệm hạch (Ganglioglioma)
*Dấu hiệu hình ảnh đặc hiệu
Hình ảnh kinh điển của u thần kinh đệm hạch (GG – ganglioglioma) là một khối dạng nang (cystic mass) với nốt đặc có thể bắt thuốc tương phản hoặc không (khoảng 50% cho thấy bắt thuốc trên CT và MRI). Hình ảnh này có lẽ chỉ xuất hiện ở khoảng một nửa số khối u, phổ biến hơn ở trẻ em. Một đặc điểm đặc trưng khác là sự hiện diện của vôi hóa, thường nằm ở ngoại vi và giống như vỏ sò (shell-like); điều này cũng được thấy ở khoảng một nửa số trường hợp.
Hầu hết u thần kinh đệm hạch (GG – ganglioglioma) xảy ra ở thùy thái dương và liên quan đến vỏ não (và do đó gây ra các cơn co giật). Thật không may, hầu hết u thần kinh đệm hạch (GG – ganglioglioma) có các đặc điểm hình ảnh không đặc hiệu và có thể được thấy ở bất cứ vị trí nào trong não, nhiều khả năng là ở tiểu não, thân não, tủy sống, giao thoa thị giác (optic chiasm), tuyến tùng, và bên trong hệ thống não thất. Kích thước của tổn thương thường từ 3 đến 6 cm tại thời điểm phát hiện. Các biểu hiện hình ảnh khác bao gồm một khối u đặc (có hoặc không bắt thuốc tương phản) và một khối tổn thương dạng thâm nhiễm.
U thần kinh đệm hạch (GG – ganglioglioma) cho thấy độ khuếch tán tương đối cao, có tín hiệu sáng trên bản đồ ADC phản ánh mật độ tế bào thấp của u. Khối u nằm ở vị trí nông có xu hướng làm mở rộng vỏ não bên trên và đôi khi MRI có thể cho thấy loạn sản vỏ não kín đáo (discreet cortical dysplasia) liên quan đến khối u. Vì chúng tồn tại nhiều năm nên xương sọ phía trên có thể biểu hiện sự tái cấu trúc của bản sọ trong. Trong các xét nghiệm y học hạt nhân bằng cả FDG và thallium, u thần kinh đệm hạch (GG – ganglioglioma) cho thấy sự hấp thu tăng cao.
Trên hình ảnh MRI phổ (MRS), u thần kinh đệm hạch (GG – ganglioglioma) biểu hiện các dấu hiệu không đặc hiệu với n-acetyl aspartate thấp, choline tăng nhẹ, creatine bình thường và myo-inositol cao trên các xét nghiệm với thời gian echo ngắn (short echo time). Lactate có thể có, thường liên quan đến hoạt động co giật gần đây.
*Thông tin lâm sàng liên quan
U thần kinh đệm hạch (GG – ganglioglioma) là một nguyên nhân thường gặp gây động kinh kháng trị (intractable epilepsy). Ganglioglioma là khối u phổ biến nhất có liên quan đến các cơn co giật thùy thái dương mạn tính (90%), chủ yếu là động kinh cục bộ phức tạp (partial complex type). Khối u phát triển rất chậm, điều này giải thích cho bản chất kéo dài của các triệu chứng. Sau khi phẫu thuật cắt bỏ, 80% bệnh nhân không còn bị co giật. Bệnh nhân mắc hội chứng Turcot (Turcot’s syndrome) có tỷ lệ mắc ganglioglioma não tăng lên.
*Chẩn đoán phân biệt
– U sao bào vàng đa hình (Pleomorphic Xanthoastrocytoma – PXA)
+ Màng não kế cận thường bắt thuốc tương phản.
+ Không có loạn sản vỏ não kèm theo
+ Khối u có thể lớn hơn nhiều.
+ Hiếm khi có vôi hóa.
– U thần kinh biểu mô loạn sản phôi (Dysembryoplastic Neuroepithelial Tumor – DNET)
+ Hình dạng “bọt xà phòng – bubbly” điển hình với nhiều nang nhỏ.
+ Không có hiệu ứng khối và phù quanh u.
+ Bắt thuốc là rất hiếm gặp
+ Có thể không phân biệt được.
– U sao bào lông (Pilocytic Astrocytoma)
+ Phần lớn xuất phát ở hố sau hoặc vùng dưới đồi.
+ Không có loạn sản vỏ não kèm theo.
+ Co giật cực kỳ hiếm gặp.
– U sao bào thâm nhiễm độ thấp (Low-Grade Infiltrative Astrocytoma (Grade II))
+ Có thể cho thấy hình ảnh thâm nhiễm nhiều hơn và giá trị ADC tương đối thấp hơn.
+ Không bắt thuốc tương phản.
+ Có thể không phân biệt được.
– U thần kinh đệm ít nhánh (Oligodendroglioma)
+ Có thể cho thấy hình ảnh thâm nhiễm nhiều hơn và giá trị ADC tương đối thấp hơn.
+ Có thể bắt thuốc tương phản và cho thấy rCBV tăng trên hình ảnh tưới máu.
+ Có thể không phân biệt được.
*Kết luận
U thần kinh đệm hạch (GG – ganglioglioma) là khối u hiếm gặp, biệt hóa tốt (well-differentiated), phát triển chậm, bao gồm các tế bào thần kinh đệm và tế bào hạch tân sinh. Loạn sản vỏ não kèm theo có thể có. Ganglioglioma chiếm khoảng 1% trong tổng số u não nguyên phát trong sọ ở người lớn và khoảng 5% ở trẻ em. Ganglioglioma có thể được thấy ở mọi lứa tuổi, nhưng có xu hướng xảy ra ở trẻ em và người trẻ tuổi. Ganglioglioma thường là khối u grade I và II theo WHO, nhưng độ ác tính hoặc chuyển dạng ác tính được thấy ở khoảng 5-10% các trường hợp. Phương pháp điều trị đầu tiên là phẫu thuật cắt bỏ kèm xạ trị và hóa trị được dành cho khối u ác tính hoặc tái phát.
Hình 1. U thần kinh đệm hạch (GG – ganglioglioma): Hình ảnh CT không tiêm thuốc tương phản mặt phẳng axial (A) ở bệnh nhân tuổi thiếu niên bị co giật cho thấy một khối u chủ yếu là giảm đậm độ không đồng nhất (mũi tên) kèm vôi hóa dạng vỏ sò (shell-like calcification) ở ngoại vi (đầu mũi tên) ở cực thái dương (temporal pole) bên phải. Ảnh hưởng đến vỏ não và các thành phần khác nhau của tổn thương được thấy trên xung T2W (B). Thành phần đặc có tín hiệu cao nhẹ (mũi tên), trong khi phù quanh u là rất nhẹ (đầu mũi tên). Có sự bắt thuốc rõ rệt của phần đặc trên xung T1W sau tiêm thuốc tương phản (C).
Hình 2. U thần kinh đệm hạch (GG – ganglioglioma): Xung FLAIR mặt phẳng coronal cho thấy một khối u ở vỏ não thùy thái dương bên phải có tín hiệu thấp (mũi tên) kèm tín hiệu cao ở ngoại vi (các đầu mũi tên). Tổn thương không bắt thuốc tương phản.
Hình 3. U thần kinh đệm hạch (GG – ganglioglioma): Xung FLAIR mặt phẳng axial (A) cho thấy một vùng vỏ não thùy thái dương bên trái có tín hiệu cao lan rộng vào chất trắng bên dưới (các mũi tên). Tổn thương làm mở rộng vỏ não và làm tái cấu trúc nhẹ bản sọ trong của xương sọ bên trên (đầu mũi tên). Xung T1W sau tiêm thuốc tương phản mặt phẳng coronal được tái tạo (B) cho thấy bắt thuốc rất ít ở phía cạnh bề mặt của khối u (các mũi tên).
Hình 4. U thần kinh đệm hạch (GG – ganglioglioma): Xung T2W mặt phẳng axial (A) cho thấy một khối u hình bầu dục, tín hiệu cao đồng nhất, giới hạn rõ (mũi tên) ở thùy trán phải. Tổn thương liên quan đến vỏ não (đầu mũi tên). Bản đồ ADC (B) cho thấy độ khuếch tán rất cao bên trong khối u. Xung T1W sau tiêm thuốc tương phản (C) cho thấy khối u không bắt thuốc (mũi tên). Có thể thấy rõ sự liên quan đến vỏ não (đầu mũi tên).
13. Nang biểu mô thần kinh (Neuroepithelial Cyst)
Hình 1. Nang biểu mô thần kinh (Neuroepithelial Cyst): Hình ảnh CT không tiêm thuốc tương phản mặt phẳng axial (A) ở bệnh nhân bị chấn thương đầu cho thấy một vùng giảm đậm độ hình bầu dục (mũi tên) ở thùy trán trái với đậm độ tương đương dịch não tủy (CSF). Xung FLAIR (B) được chụp để theo dõi tổn thương này cho thấy một vùng có giới hạn rõ (mũi tên) đồng tín hiệu với dịch não tủy và chỉ có bất thường tín hiệu rất ít và khu trú ở ngoại vi. Bản đồ ADC tương ứng (C) cho thấy độ khuếch tán rất cao bên trong nang bằng với dịch não tủy. Xung T1W mặt phẳng sagittal không tiêm thuốc tương phản (D) cho thấy nang có các ngăn nhỏ bên trong (mũi tên).
Hình 2. Nang biểu mô thần kinh (Neuroepithelial Cyst): Xung T2W mặt phẳng axial (A) cho thấy một tổn thương nằm ở sâu của thùy trán bên phải có giới hạn rõ và đa thùy (mũi tên) với tín hiệu giống dịch não tủy (CSF), không có phù hoặc hiệu ứng khối. Xung T1W mặt phẳng coronal sau tiêm thuốc tương phản (B) cho thấy vùng giống dịch não tủy này (CSF-like area) không bắt thuốc (mũi tên).
Hình 3. Nang biểu mô thần kinh (Neuroepithelial Cyst): Xung T2W FS (xóa mỡ) (A) cho thấy một khối tổn thương hình bầu dục giống dịch não tủy (CSF) (mũi tên) xuất phát tại vị trí nằm kế cận hoặc từ hồi hải mã (đầu mũi tên). Vị trí bệnh lý đặc trưng của nang (mũi tên trắng) nằm phía trong hồi hải mã (mũi tên đen) được thể hiện rõ trên xung T1W mặt phẳng coronal sau tiêm thuốc tương phản (B). Ghi nhận khe màng mạch (choroidal fissure) đối bên (đầu mũi tên).
14. U sao bào khổng lồ dưới màng não thất (Subependymal Giant Cell Astrocytoma – SEGA)
Figure 1. U sao bào khổng lồ dưới màng não thất (Subependymal Giant Cell Astrocytoma – SEGA): Axial T1WI (A) in a 9-year-old girl shows an isointense multilobulated mass (arrow) at the left foramen of Monro and multiple tiny subependymal nodules (arrowheads). The mass (arrow) homogenously enhances on the postcontrast image (B), and is similar to the gray matter on ADC map (C). The small nodules do not enhance. Coronal T2WI (D) reveals the isointensity of the mass (arrow) as well as inferior cystic portions abutting the third ventricle. There is diffuse hyperintensity of the left basal nuclei (*).
Figure 2. U sao bào khổng lồ dưới màng não thất (Subependymal Giant Cell Astrocytoma – SEGA): Non-enhanced CT in a teenage boy shows partially calcified masses at foramina of Monro (arrows). There are smaller calcified lesions (arrowheads) along bilateral thalamocaudate sulcus.
Figure 3. U sao bào khổng lồ dưới màng não thất (Subependymal Giant Cell Astrocytoma – SEGA): MRI in a newborn shows typical neonatal characteristics of bilateral lesions (arrows) at the foramina of Monro: hyperintense on T1WI (A), hypointense on T2WI (B), and with low ADC values (D). This signal pattern is similar to that of a left parietal tuber (arrowhead) and is consistent with hypermyelination.
15. U dưới màng não thất (Subependymoma)
Figure 1. U dưới màng não thất (Subependymoma): Axial FLAIR image (A) shows a very bright lesion (arrow) in the left lateral ventricle, just above the foramen of Monro, without mass effect or surrounding edema. The mass (arrow) is slightly hypointense and shows no enhancement on corresponding post-contrast T1WI (B). ADC map (C) reveals increased intralesional diffusivity (arrow). The mass (arrow) exhibits very low blood volume on perfusion MRI (D).
Figure 2. U dưới màng não thất (Subependymoma): Non-enhanced CT image reconstructed in the sagittal plane (A) shows a small isodense lesion (arrow) in the inferior aspect of the fourth ventricle. Axial CT image (B) shows a small internal calcification (arrow) to a better advantage. The oval mass (arrow) is mildly hyperintense and heterogenous on T2WI (C). There was no lesion enhancement on post-contrast images (not shown).
Figure 3. U dưới màng não thất (Subependymoma): FLAIR image (A) reveals a very bright intraventricular lesion (arrow) adjacent to the right foramen of Monro (arrowhead). The mass (arrow) is overall hyperintense and mildly heterogenous on corresponding T2WI (B), with small bright and dark areas. The lesion shows a focal area of internal enhancement (arrowhead) on post-contrast T1WI (C).
16. U màng não thất (Ependymoma)
Figure 1. U màng não thất (Ependymoma): Non-enhanced axial CT image (A) shows a posterior fossa mass (arrows) with dense calcifications (arrowheads). ADC map obtained at a different angle (B) reveals mildly increased diffusion of the lesion (arrows). The mass (arrow) is heterogenous on T2WI (C) and its hypointense portion (arrowhead) extends through the foramen of Luschka. There is avid lesion enhancement (arrow) on post-contrast T1WI (D).
Figure 2. U màng não thất (Ependymoma): Sagittal T1WI without contrast (A) shows a heterogenous hypointense mass (arrow) filling the fourth ventricle and extending inferiorly through the foramen of Magendie (arrowhead). Axial T2WI (B) shows the heterogenously hyperintense mass (arrows) expanding the fourth ventricle and extending through the left foramen of Luschka (arrowhead).
Figure 3. U màng não thất (Ependymoma): Axial T1WI without contrast (A) shows a heterogenous mass (arrow) along the margin of the left lateral ventricle with a presumed large cystic portion (*). The cystic area (*) is hyperintense to the CSF on FLAIR (B) indicating proteinaceous contents. There is mild surrounding edema (arrowheads). Post-contrast T1WI (C) reveals heterogenous enhancement (arrows) of the solid portions.
17. U sao bào lông (Pilocytic Astrocytoma)
Figure 1. U sao bào lông (Pilocytic Astrocytoma): Axial T2WI (A) shows a well-defined cerebellar mass (arrow) with hyperintense solid and cystic (*) components. Corresponding pre-contrast T1WI (B) shows low signal of the solid component (arrow). ADC map (D) reveals increased diffusion within the solid portion (arrow) compared to the normal brain. Post-contrast T1WI (C) shows intense enhancement of the solid component (arrow) and cyst wall (arrowheads).
Figure 2. U sao bào lông (Pilocytic Astrocytoma): Axial non-enhanced CT image (A) in a 9-year-old boy with headache and vomiting shows a predominantly hypodense mass (arrow) in the supravermian cistern. Enhanced CT image (B) reveals partial enhancement (arrowheads) of this lesion. ADC map at a similar level (C) demonstrates bright signal consistent with very high diffusion within the mass (arrow).
Figure 3. U sao bào lông (Pilocytic Astrocytoma): Axial T2WI (A) shows a bright posterior fossa mass (arrow) centered at the fourth ventricle. The lesion (arrow) is also very bright on ADC map (B), while post-contrast T1WI (C) reveals partial and heterogenous enhancement (arrowheads).
18. U nguyên bào tủy (Medulloblastoma)
Figure 1. U nguyên bào tủy (Medulloblastoma): Axial non-enhanced CT image in a 5-year-old child shows a hyperdense midline cerebellar mass (arrow) located adjacent to the fourth ventricle (arrowhead).
Figure 2. U nguyên bào tủy (Medulloblastoma): On axial T2WI (A) in another patient, the fourth ventricle is filled with a mass that consists of slightly hyperintense strands (arrow) and bright oval portions (arrowheads). The strands (arrow) are darker than the brain on ADC map (B), consistent with solid tissue. The very bright components (arrowheads) are similar to the CSF and globes (*) and consistent with cysts.
Figure 3. U nguyên bào tủy (Medulloblastoma): Midsagittal post-contrast T1WI (A) shows mild to moderate primarily linear enhancement of the fourth ventricle mass (arrow). Axial T2WI (B) reveals mild hyperintensity of the lesion (arrow) and apparent cystic components (arrowheads). Corresponding ADC map (C) shows low diffusivity within the solid portion of the mass (arrow). Diffusivity within the cysts (arrowheads) is similar to that of the CSF.
Figure 4. U nguyên bào tủy (Medulloblastoma): Non-enhanced axial CT image (A) shows a hyperdense mass (arrow) almost completely filling the fourth ventricle (arrowhead). Post-contrast sagittal T1WI (B) shows heterogenous enhancement of the mass (arrow). There are multiple additional enhancing lesions (arrowheads) along the surface of the brain and spinal cord, consistent with leptomeningeal spread.
19. U nguyên bào mạch máu (Hemangioblastoma)
Figure 1. U nguyên bào mạch máu (Hemangioblastoma): Axial T2WI (A) shows a very bright cerebellar mass (arrows) and multiple flow-voids (arrowheads) located within and along the edges of the lesion. Surrounding edema is also seen. Corresponding ADC map (B) reveals very high signal of the lesion (arrows), consistent with high diffusivity, similar to the signal of the surrounding edema (arrowheads). Matching post-contrast T1WI (C) demonstrates marked homogenous enhancement of the mass (arrow). Some internal flow-voids are still visible (arrowheads).
Figure 2. U nguyên bào mạch máu (Hemangioblastoma): Sagittal pre-contrast T1WI (A) in a 41-year-old patient with headache and dizziness shows a CSF-like hypointense cerebellar mass (arrow) with an eccentric isointense nodule (arrowhead). Matching post-contrast T1WI (B) shows marked enhancement of the mural nodule (arrowhead), which has a large base at the cerebellar surface. The rest of the mass remains CSF-like, consistent with a cyst. The cyst wall does not enhance.
Figure 3. U nguyên bào mạch máu (Hemangioblastoma): Axial post-contrast T1WI (A) shows two enhancing lesions (arrows) and a cyst with enhancing mural nodule (arrowhead). Small solid cerebellar tumors are not conspicuous on pre-contrast T1WI (B).
Figure 4. U nguyên bào mạch máu (Hemangioblastoma): T2WI (A) shows a left cerebellar mass (white arrow) with flow-voids (arrowheads) and adjacent edema (black arrow). The mass (arrow) is bright on ADC map (B) and has high CBV on perfusion MRI (C).
20. Khối u có xuất huyết (Hemorrhagic Neoplasms)
Figure 1. Khối u có xuất huyết (Hemorrhagic Neoplasms): Unenhanced CT image (A) shows a right temporal hematoma (arrow) with surrounding hypodense edema. A slightly more cephalad T2WI (B) reveals heterogeneous signal within the lesion with irregular and discontinuous hemosiderin ring (arrowheads). Corresponding post-contrast T1WI (C) shows irregular and in places nodular (arrows) peripheral enhancement of the lesion.
Figure 2. Khối u có xuất huyết (Hemorrhagic Neoplasms): Unenhanced CT image (A) in a patient with breast cancer shows a hemorrhagic lesion in the right cerebellum. Note fluid level (arrowhead) and a small nodular focus (arrow). Corresponding post-contrast T1WI (B) reveals thick enhancement around the nodule (arrows).
Figure 3. Khối u có xuất huyết (Hemorrhagic Neoplasms): Unenhanced CT (A) in a patient with melanoma shows bilateral heterogenous hemorrhages – right frontal lesion (arrow) has an irregular, lobulated contour; left parietal hematoma (arrowhead) is slightly darker and likely to be older. Corresponding pre-contrast T1WI (B) and T2WI (C) show iso- to slightly hyperintense signal in the frontal lesion, indicating more acute hemorrhage. The left parietal lesion contains predominantly central T1 hyperintense areas (arrowhead) suggesting subacute clot (methemoglobin), and concentric internal ring of low T2 signal (arrow) suggesting repeated hemorrhages (hemosiderin).
Tài liệu tham khảo:
Brain Imaging with MRI and CT: An Image Pattern Approach (p317,…)
Người dịch: Bs. Lê Thị Ny Ny – Anhvanyds.
Để lại một phản hồi Hủy