Sự bùng phát của SARS-CoV-2 đã gây ra đại dịch đầu tiên của thế kỷ. SARS-CoV-2 chủ yếu lây truyền qua các giọt bắn, các con đường lan truyền khác vẫn còn là giả thuyết chưa được xác nhận. Cho đến nay, vẫn chưa rõ liệu SARS-CoV-2 có thể lây truyền từ mẹ sang thai nhi hay không và nếu có thì bằng cách nào.
Trong báo cáo này, chúng tôi chứng minh sự lây truyền SARS-CoV-2 qua nhau thai từ người mẹ bị nhiễm bệnh trong 3 tháng cuối thai kỳ sang cho trẻ kèm theo các biểu hiện tổn thương thần kinh ở trẻ. Sự lây nhiễm này đã được xác nhận bằng các cuộc điều tra toàn diện về virus và bệnh lý. Cụ thể, SARS-CoV-2 gây ra: (1) nhiễm virus trong máu mẹ, (2) nhiễm trùng nhau thai được chứng minh bằng hoá mô miễn dịch và tải lượng virus rất cao; viêm nhau thai được cho thấy qua các xét nghiệm chẩn đoán mô bệnh học và hoá mô miễn dịch và (3) nhiễm virus ở trẻ sơ sinh sau nhiễm trùng nhau thai. Trẻ sơ sinh được nghiên cứu trên lâm sàng, thông qua các xét nghiệm chẩn đoán hình ảnh và theo dõi. Trẻ xuất hiện các biểu hiện thần kinh, tương tự các triệu chứng đã từng được mô tả ở người lớn nhiễm bệnh.
Nhiễm SARS-CoV-2 gây dịch bệnh coronavirus mới (COVID-19), chủ yếu lan truyền qua các giọt bắn, các con đường lây nhiễm khác mới chỉ là giả thuyết được đặt ra. Một số trường hợp lây nhiễm chu sinh đã được mô tả nhưng đường lây không rõ là qua nhau thai, qua cổ tử cung hay do tiếp xúc với môi trường. Điều quan trọng là phải làm rõ liệu SARS-CoV-2 có đến được thai nhi hay không và nếu có thì bằng cách nào nhằm ngăn ngừa tình trạng nhiễm trùng sơ sinh, tối ưu hoá quản lý thai kỳ và cuối cùng là để hiểu rõ hơn về sinh học SARS-CoV-2. Ở đây chúng tôi trình bày một ca lâm sàng toàn diện cho thấy sự lây truyền SARS-CoV-2 qua nhau thai với các biểu hiện thần kinh ở trẻ sơ sinh, phù hợp với các dấu hiệu và triệu chứng thần kinh của COVID-19.
Kết quả
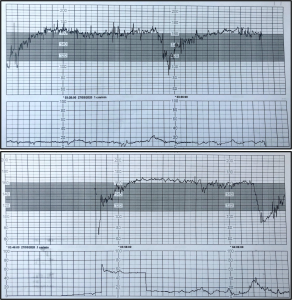
Ca lâm sàng: Thai phụ 23 tuổi, G1P0, thai 35 tuần 2 ngày, vào viện tháng 3 năm 2020 vì ho khạc đờm nhiều từ 2 ngày trước khi nhập viện. Xét nghiệm PCR được tiến hành như mô tả trong phần Phương pháp bên dưới: cả gen E và S của SARS-CoV-2 đều được phát hiện trong các mẫu bệnh phẩm máu, dịch tỵ hầu và dịch tiết âm đạo. Quá trình mang thai không phát hiện thấy bất thường và tất cả các lần siêu âm, kiểm tra định kỳ đều bình thường cho đến khi bệnh nhân được chẩn đoán mắc COVID-19. Kết quả xét nghiệm của thai phụ khi nhập viện: giảm tiểu cầu (54 x 109 G/l), giảm bạch cầu lympho (0,54 x 109 G/l), APTT kéo dài (60s), tăng men gan (AST 81 IU/l; ALT 41 IU/l), tăng CRP (37mg/l) và ferritin (431 Mg/l). Sau 3 ngày nhập viện, thai phụ được theo dõi nhịp tim thai thấy biểu đồ loại III (Hình 1) và do đó được tiến hành mổ lấy thai (https:// www.rcog.org.uk/globalassets/documents/guidelines/goodpractice 11classificationofurgency.pdf) với màng ối còn nguyên vẹn, được cách ly hoàn toàn và gây mê toàn thân do có các triệu chứng hô hấp. Nước ối trong được lấy mẫu làm xét nghiệm trước khi vỡ màng ối, trong khi mổ lấy thai và cho kết quả dương tính với cả gen E và gen S của SARS-CoV-2. Không tiến hành kẹp rốn muộn do nguy cơ lây truyền SARS-CoV-2 qua đó chưa được biết rõ. Thai phụ vẫn ở lại viện để theo dõi trên lâm sàng và cuối cùng 6 ngày sau khi sinh, thai phụ xuất viện trong tình trạng sức khoẻ ổn định.
| Bảng 1: Các xét nghiệm chính ở trẻ sơ sinh | ||||
| 1 ngày tuổi | 2 ngày tuổi | 3 ngày tuổi | 5 ngày tuổi | |
| Tổng phân tích tế bào máu | ||||
| WBC/L | 10,32 x 109 | 6,97 x 109 | ||
| RBC/L | 4,54 x 1012 | 4,84 x 1012 | ||
| Hb (g/dL) | 13,9 | 14,7 | ||
| HCT (%) | 41,6 | 41,4 | ||
| PLT/L | 339 x 109 | 319 x 109 | ||
| Lymphocytes/L | 4,39 x 109 | 3,05 x 109 | ||
| Neutrophils/L | 3,97 x 109 | 2,78 x 109 | ||
| Hồng cầu lưới (%) | 3,04 | 3,39 | ||
| Xét nghiệm khí máu | ||||
| pH | 7,27 | 7,38 | 7,34 | |
| pCO2 (mmHg) | 41 | 41 | 47 | |
| pO2 (mmHg) | 41 | 40 | 30 | |
| BE (mmol/L) | -7,8 | -1,4 | -1 | |
| Lactate (mmol/L) | 7 | 1,3 | 1,5 | |
| Na (mmol/l) | 135 | 141 | 141 | |
| K (mmol/l) | 6,3 | 5,2 | 4,3 | |
| Cl (mmol/l) | 109 | 110 | 110 | |
| Ca++ (mmol/l) | 1,08 | 1,33 | 1,38 | |
| Sinh hoá máu | ||||
| CRP (mg/L) | < 5 | < 5 | ||
| PCT (Mg/L) | 0,95 | 0,61 | ||
| PCT máu cuống rốn (Mg/L) | 0,19 | |||
| Bilirubin toàn phần trong huyết thanh (Mmol/L) | 106 | |||
| Bilirubin liên hợp trong huyết thanh (Mmol/L) | 0 | |||
| ALP (IU/L) | 133 | |||
| AST (IU/L) | 38 | |||
| ALT (IU/L) | 9 | |||
| -GT (IU/L) | 290 | |||
| Troponine I (ng/L) | 43 | |||
| Xét nghiệm dịch não tuỷ | ||||
| Protein (g/L) | 1,49 | 1,24 | ||
| Tế bào bạch cầu/mm3 | 300 | 11 | ||
| Glucose (mmol/L) | 2,9 | 2,4 | ||
| Tất cả các mẫu bệnh phẩm đều được lấy từ máu tĩnh mạch, ngoại trừ khí máu được thực hiện trên các mẫu máu mao mạch hoá động mạch khi lấy máu gót chân đã được ủ ấm. Các phép đo lường được tiến hành bằng các phương pháp phân tích vi mô được chứng nhận dành riêng cho NICU và tuân thủ các kiểm soát chất lượng định kỳ. Tất cả kết quả đều bình thường trong khoảng tham chiếu của trẻ sơ sinh, ngoại trừ protein và số lượng tế bào bạch cầu trong dịch não tuỷ ở ngày thứ 3 sau sinh; nồng độ glucose trong dịch não tuỷ luôn tương đương với nồng độ glucose trong máu được xét nghiệm cùng thời điểm. | ||||
Virus và bệnh học: RT-PCR trên nhau thai dương tính với cả 2 gen SARS-CoV-2. Hình 3 cho biết tất cả các kết quả RT-PCR thu được từ các mẫu bệnh phẩm khác nhau của mẹ và trẻ sơ sinh: tải lượng virus trong mô nhau thai cao hơn nhiều so với trong nước ối và các mẫu máu xét nghiệm từ mẹ và trẻ sơ sinh.
Xét nghiệm chẩn đoán mô bệnh học nhau thai được thực hiện như mô tả trong phần Phương pháp bên dưới và cho thấy sự lắng đọng fibrin quanh gai nhau lan toả kèm theo nhồi máu và tình trạng viêm gian gai nhau cấp tính, mạn tính. Màng bào tương các tế bào nuôi quanh gai nhau dương tính mạnh và lan toả khi nhuộm hoá mô miễn dịch với kháng thể kháng protein N của SARS-CoV-2. Không phát hiện tác nhân gây bệnh nào khác trên nhuộm đặc biệt và hoá mô miễn dịch. Hình 4 và hình 5 mô tả kết quả khi khảo sát đại thể và vi thể cũng như hoá mô miễn dịch nhau thai.
Bàn luận
Chúng tôi báo cáo một trường hợp đã được chứng minh về sự lây truyền SARS-CoV-2 qua nhau thai từ sản phụ nhiễm COVID-19 sang con ở cuối thai kỳ. Các ca bệnh khác có khả năng lây truyền chu sinh đã được mô tả gần đây nhưng còn một số vấn đề vẫn chưa được làm sáng tỏ. Ví dụ, một số ca bệnh không phát hiện được SARS-CoV-2 ở trẻ sơ sinh hoặc chỉ báo cáo sự có mặt của các kháng thể đặc hiệu; số khác tìm thấy virus trong các mẫu bệnh phẩm của trẻ sơ sinh nhưng không rõ đường lây truyền vì nhau thai, nước ối, máu mẹ và trẻ sơ sinh không được làm xét nghiệm một cách hệ thống ở mỗi cặp mẹ-con.
Một bảng phân loại xác định các trường hợp nhiễm SARS-CoV-2 ở phụ nữ có thai, thai nhi và trẻ sơ sinh đã được công bố gần đây và chúng tôi đề xuất dựa vào đó để mô tả các trường hợp có khả năng lây truyền SARS-CoV-2 chu sinh. Theo hệ thống phân loại này, nhiễm trùng bẩm sinh ở trẻ sơ sinh được chứng minh khi phát hiện thấy virus trong nước ối được lấy mẫu trước khi vỡ ối hoặc trong máu được lấy mẫu ngay sau sinh, vì vậy, trường hợp của chúng tôi hoàn toàn đủ tiêu chuẩn để chẩn đoán lây nhiễm SARS-CoV-2 bẩm sinh, trong khi các ca bệnh kể trên chỉ được phân loại là có khả năng hoặc thậm chí không có khả năng nhiễm bệnh. Một báo cáo khác gần đây mô tả một ca bệnh có các đặc điểm nhau thai tương tự nhưng chỉ được phân loại là có khả năng nhiễm SARS-CoV-2 bẩm sinh vì không thể xét nghiệm máu và cuống rốn của trẻ sơ sinh.
Cả gen E và gen S của SARS-CoV-2 đều được tìm thấy trong mỗi mẫu bệnh phẩm, do đó chúng đều được coi là dương tính theo các khuyến cáo của Trung tâm Kiểm soát Dịch bệnh Châu Âu (https://www.ecdc.europa.eu/en/all-topics-z/coronavirus/threats- and-outbreaks/covid-19/laboratory-support/questions). Đáng chú ý, tải lượng virus trong mô nhau thai cao hơn nhiều so với trong nước ối và máu mẹ: điều này cho thấy sự có mặt của virus trong các tế bào nhau thai, phù hợp với các đặc điểm của tình trạng viêm khi xét nghiệm chẩn đoán mô bệnh học. Cuối cùng, đường cong RT-PCR của mẫu bệnh phẩm dịch tỵ hầu vào ngày thứ 3 và 18 sau sinh của trẻ cao hơn ngày đầu tiên (khi trẻ được cách ly hoàn toàn trong phòng áp lực âm): đây cũng là một xác nhận khác cho chúng ta thấy tình trạng nhiễm trùng sơ sinh thực sự hơn là sự nhiễm bẩn. Do đó, những phát hiện này gợi ý rằng: (1) mẹ nhiễm virus và virus đã đến nhau thai được chứng minh bằng hoá mô miễn dịch; (2) virus gây ra phản ứng viêm đáng kể được thể hiện qua tải lượng virus rất cao, xét nghiệm chẩn đoán mô bệnh học và hoá mô miễn dịch; (3) trẻ sơ sinh nhiễm virus sau nhiễm trùng nhau thai. Các phát hiện của chúng tôi cũng phù hợp với một ca bệnh mô tả sự có mặt của các virion (hạt virus) trong mô nhau thai mặc dù trường hợp này không báo cáo về tình trạng viêm nhau thai cũng như tình trạng nhiễm trùng thai nhi/nhiễm trùng sơ sinh.
Nhau thai cho thấy các dấu hiệu viêm gian gai nhau cấp tính và mạn tính phù hợp với tình trạng viêm hệ thống nghiêm trọng của sản phụ do nhiễm SARS-CoV-2. Vì RT-PCR trên mô nhau thai và các mẫu bệnh phẩm từ máu mẹ và trẻ sơ sinh đều dương tính với SARS-CoV-2, sự lây truyền qua nhau thai rõ ràng đã xảy ra. Điều thú vị là, nhau thai của những sản phụ nhiễm SARS-CoV-1 cho thấy những đặc điểm bệnh lý viêm gian gai nhau tương tự, cùng với sự lắng đọng fibrin giữa các gai nhau. Enzyme chuyển Angiotensin 2 (ACE2) là thụ thể của SARS-CoV-2 và được biểu hiện cao trong các mô nhau thai. Dữ liệu trên động vật cho thấy sự biểu hiện ACE2 thay đổi trong các mô thai nhi/trẻ sơ sinh theo thời gian và đạt đỉnh trong khoảng từ cuối thai kỳ đến những ngày đầu sau sinh. Sự kết hợp các dữ liệu này và các phát hiện của chúng tôi khẳng định sự lây truyền qua nhau thai thực sự có thể xảy ra trong những tuần cuối của thai kỳ mặc dù chúng ta không thể loại trừ khả năng lây truyền và các hậu quả cho thai nhi sớm hơn trong thai kỳ vì vẫn chưa có dữ liệu rõ ràng.
Điều thú vị là, chúng tôi mô tả một trường hợp nhiễm trùng bẩm sinh kèm theo các biểu hiện thần kinh sau nhiễm virus ở trẻ sơ sinh. Trẻ sơ sinh nghi nghiễm SARS-CoV-2 có các triệu chứng không đặc hiệu hoặc viêm phổi trong khi các triệu chứng thần kinh thường thấy ở các bệnh nhân người lớn, đặc biệt do đáp ứng viêm. Các biểu hiệu thần kinh sớm cũng đã được quan sát ở một trẻ sơ sinh khác có mẹ dương tính với SARS-CoV-2, mặc dù sự lây truyền dọc chưa được nghiên cứu đầy đủ. Ngược lại, sau khi nhiễm virus, trường hợp của chúng tôi biểu hiện rõ ràng các triệu chứng thần kinh và các dấu hiệu viêm trong dịch não tuỷ. Không có tình trạng nhiễm vi khuẩn, virus nào khác và tất cả các rối loạn sơ sinh khác có khả năng gây ra các triệu chứng lâm sàng này đều đã được loại trừ. Hình ảnh học thần kinh liên tục chỉ ra tổn thương chất trắng, có thể gây ra bởi tình trạng viêm mạch máu do nhiễm SARS-CoV-2 trong khi những hình ảnh tương tự đã được tìm thấy đơn lẻ ở các bệnh nhân người lớn
Kết luận, chúng tôi đã chứng minh rằng sự lây truyền SARS-CoV-2 qua nhau thai có thể xảy ra trong suốt các tuần cuối của thai kỳ. Sự lây truyền qua nhau thai có thể gây viêm nhau thai và nhiễm virus ở trẻ sơ sinh. Trẻ cũng có thể kèm theo các triệu chứng thần kinh do viêm mạch máu não.
Hình 3: Kết quả RT-PCR. a, b Các gen A và S của SARS-CoV-2 lần lượt cho mẫu bệnh phẩm của mẹ và trẻ sơ sinh (trục X và Y lần lượt biểu diễn lượng ARN được khuếch đại và số chu kỳ; tín hiệu được phát hiện càng sớm, số chu kỳ càng ít và tải lượng virus càng cao). c Tải lượng virus cho mỗi mẫu bệnh phẩm (được biểu thị bằng Log bản sao/triệu tế bào nhau thai và Log bản sao/ml cho tất cả các mẫu bệnh phẩm khác). Tất cả các mẫu xét nghiệm từ mẹ đều được lấy ngay trước sinh hoặc trong khi mổ lấy thai; các mẫu bểnh phẩm từ trẻ sơ sinh được liệt kê theo thời gian và lấy mẫu từ ngày đầu tiên đến ngày thứ 3 sau sinh, ngoại trừ mẫu bệnh phẩm dịch tỵ hầu cuối cùng (lấy vào ngày 18 sau sinh). Các đường màu hiển thị kết quả của xét nghiệm RT-PCR cho mỗi mẫu bệnh phẩm. Đường màu cam đậm thể hiện chứng dương, là dịch nổi trong môi trường nuôi cấy SARS-CoV-2 (chi tiết hơn trong “Phương pháp”). Mẫu bệnh phẩm dịch tỵ hầu ngày thứ 1, 3 và 18 sau sinh được biểu thị lần lượt bằng các đường cong màu cam, xám và xanh lá cây. Tải lượng virus trong dịch rửa phế quản phế nang không được thể hiện.
Phương pháp
Lấy mẫu bệnh phẩm. Các mẫu sinh học làm xét nghiệm RT-PCR được lấy và chuẩn bị như sau. Lấy dịch tỵ hầu và dịch tiết âm đạo theo hướng dẫn của Trung tâm Kiểm soát và Phòng ngừa Dịch bệnh Hoa Kỳ (https://www.cdc.gov/ symptoms due to cerebral vasculitis may also be associated. Methods Patient sampling. Biological samples to be tested by RT-PCR were obtained and prepared as follows. Nasopharyngeal and vaginal swabs were obtained following coronavirus/2019-ncov/hcp/inpatient-obstetric-healthcare-guidance.html; https:// www.cdc.gov/groupbstrep/downloads/gbs_swab_sheet21.pdf). Lấy một mẫu mô nhau thai từ phía màng đệm và nghiền trong 400ml nước không chứa RNAase và DNAase; đặt 1ml máu và tăm bông chứa bệnh phẩm trong môi trường vận chuyển virus Virocult® (Sigma, St. Louis, MI, USA). Rửa phế quản phế nang không qua nội soi (BAL) được thực hiện theo một kỹ thuật tiêu chuẩn phổ biến: cụ thể, đặt trẻ sơ sinh nằm ngửa với đầu quay sang phải, vì vậy mẫu bệnh phẩm được lấy chủ yếu ở bên phổi trái. Nhỏ nước muối đẳng trương (1 ml/kg, 370C) vào trong ống nội khí quản qua một chạc ba. Sau 3 chu kỳ thông khí, đưa nhẹ nhàng ống hút đờm vào sâu 0,5cm và hút dịch đường thở vào lọ đựng bệnh phẩm (BALF Trap; Vigon, Ecouen, France) với áp lực âm 50mmHg. Quy trình này được lặp lại khi cho trẻ quay đầu sang trái, khi đó mẫu bệnh phẩm được lấy chủ yếu ở bên phổi phải. Quy trình tuân theo hướng dẫn lấy dịch rửa phế quản phế nang cho trẻ em và trẻ sơ sinh của Hiệp hội Hô hấp Châu Âu. Trong suốt quy trình, bệnh nhân không bao giờ được ngưng thở máy, nồng độ oxy trong khí hít vào (FiO2) 0,25 và không có tình trạng giảm bão hoà oxy hay nhịp tim chậm. Tất cả các mẫu bệnh phẩm đều được bảo quản ở +40C và làm xét nghiệm trong vòng 24 giờ.
Phản ứng tổng hợp chuỗi thời gian thực (RT-PCR). RNA virus được tách từ 200Ml mẫu bệnh phẩm trên lâm sàng bằng NucliSENS® easyMag® (BioMérieux, Craponne, France) và được rửa trong 100Ml. RealStar® SARS-CoV-2 RT-PCR Kit 1.0 (Altona Diagnostics GmbH, Hamburg, Germany) đánh dấu gen E (đặc hiệu cho B-betacoronavirus) và gen S (đặc hiệu cho SARS-CoV-2) theo khuyến cáo của nhà sản xuất (http://(https://altona-diagnostics.com/en/products/ reagents-140/reagents/realstar-real-time-pcr-reagents/realstar-sars-cov-2-rt-pcr- kit-ruo.html). Xét nghiệm bao gồm một hệ thống khuếch đại các dòng khác (chứng nội tại) để xác định khả năng ức chế RT-PCR và xác nhận tình trạng nguyên vẹn của thuốc thử trong bộ xét nghiệm. Chứng dương là dịch nổi trong môi trường nuôi cấy SARS-CoV-2 được cung cấp bởi nhà sản xuất bộ xét nghiệm. Chu kỳ nhiệt được thực hiện ở 550C trong 20 phút đối với phiên mã ngược, tiếp theo là 950C trong 2 phút và sau đó là 45 chu kỳ ở 950C trong 15 giây, 550C trong 45 giây, 720 trong 15 giây với Applied Biosystems ViiA7 instrument (Applied Biosystems, Thermo Fisher, Waltham, MA, USA). Giá trị chu kỳ ngưỡng nhỏ hơn 40 được hiểu là dương tính với SARS-CoV-2 RNA. Kỹ thuật này giúp chúng tôi có giới hạn phát hiện cực thấp (LOD = 1200 cp/mL (12 cp/rxn)). Khả năng tái sản xuất và sự thống nhất giữa các xét nghiệm đều đạt 100% với cả xét nghiệm âm tính và dương tính, so với hai kỹ thuật phổ biến khác.
Kiểm tra nhau thai. Lấy mẫu xét nghiệm nhau thai, tiến hành khảo sát đại thể và vi thể theo tuyên bố đồng thuận Amsterdam. Nhau thai được cố định trong đệm formalin và vùi trong paraffin. Các phương pháp nhuộm được thực hiện trên các phần dày 3-5Mm: haemalun eosin saffran, periodic acid schiff and Gomori-Grocott stains. Hoá mô miễn dịch với với phát hiện peroxydase và nhuộm hemalun trong máy hoá mô miễn dịch tự động Leica Bond III sử dụng bộ xét nghiệm Bond Polymer Refine Detection (Leica DS9800) sau khi tiền xử lý nhiệt ở pH 6 hoặc 9 tuỳ thuộc vào các kháng thể đơn dòng được xét nghiệm: D68 (Dako PG-M1, 1:200), CD163 (Leica 10D6, 1:200), CD20 (Dako L26, 1:400), CD3 (Dako F7.2.38, 1:50), CD5 (Novocastra 4C7, 1:50), CMV (Dako CCH2 + DDG9, 1:1), Parvo virus (AbcVs, Abc10-P038), SARS-CoV-2 (Abclonal, rabbit pAB, 2019- nCoV N Protein, 1:2400). Hoá mô miễn dịch chứng âm của SARS-CoV-2 được thực hiện: chứng từ kháng thể sơ cấp đa dòng của thỏ, mẫu bệnh phẩm nhau thai âm tính với SARS-CoV-2 kèm theo các điều kiện cố định bằng formalin tương tự trước khi phân tích.
Tài liệu tham khảo
https://www.nature.com/articles/s41467-020-17436-6?fbclid=IwAR3tO0uoISdxzhi03doRcnW5bxtZxt-4kUqr0oBQDYBaxfz-hlkZ3Fu5KpA
Bác sỹ Đỗ Hồng Phương
Khoa Nội Nhi Tổng hợp Bệnh viện E
Để lại một phản hồi Hủy